キヤノンITソリューションズ(キヤノンITS)は10月9日、スマートデバイスを利用した製薬企業向け営業支援システム「PVLink Camera Report(ピーブイリンクカメラレポート)」の新バージョンの販売を開始した。価格は、いずれも税別でベースライセンス(100人分のMRライセンス含む)が300万円、MRライセンスが(100人)が50万円。
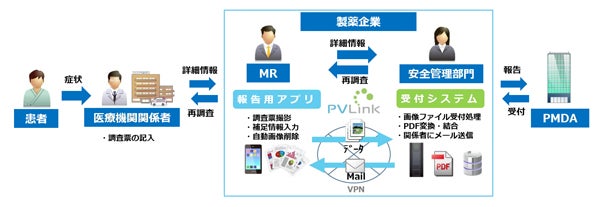
PVLink Camera Reportは、製薬企業のMR(医薬情報担当者)が、医療機関から収集した医薬品の副作用・症例情報の紙ベースの調査票をスマートデバイスのカメラで撮影して電子化し、自社の安全管理部門に迅速かつセキュアに報告するシステム。
新バージョンでは従来の医薬品の副作用・症例報告に加え、医療機器の不具合報告にも対応するとともに安全管理部門がとりまとめている安全性情報進捗管理システムへの自動登録機能を搭載し、多忙なMRと安全管理部門の業務負荷を軽減するという。
医薬品の副作用・感染症の情報および医療機器の不具合などの情報は、安全確保を図るため厚生労働省所管のPMDA(医薬品医療機器総合機構)への迅速な報告が必要になるという。そのため、新バージョンでは従来の紙帳票の電子化機能に加え、新たに汎用撮影モードを搭載し、医療機器(ex.CT装置や心電計、注射器など)の不具合報告業務に対応した。
これにより、従来のFAXやEメールを使用した報告による宛先間違いや、誤ったデータを配信してしまうなどの人為ミスを防止し、都度手作業で送信する必要があるなど、運用上の課題を解決することができるほか、撮影対象や撮影環境に応じて画像品質を調整できる機能を追加し、医療機器の破損や不具合状況の視認性も向上した。
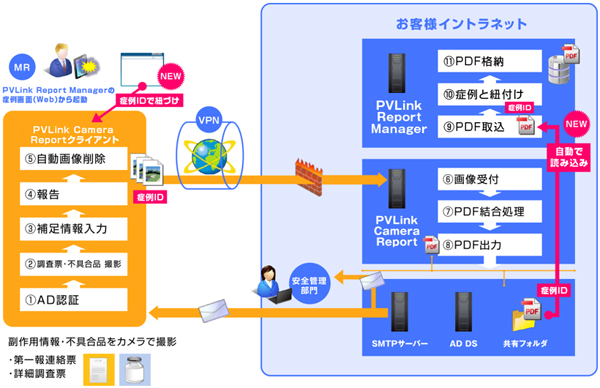
そのほか、PVLink Camera Reportと同社が提供する安全性情報進捗管理システム「PVLink Report Manager」との連携機能を強化することで、MRが調査した副作用・感染症の詳細調査結果を当該症例に紐づけて自動登録、進捗管理を可能としている。
PVLink Camera Reportからの報告PDFを「PVLink Report Manager」が症例IDをもとに自動で読み込んで一元管理するため、安全管理部門が手動で登録する必要がなくなり、報告遅延や報告漏れを防ぐことも可能とし、PMDAへの副作用報告を円滑に行うことができるという。
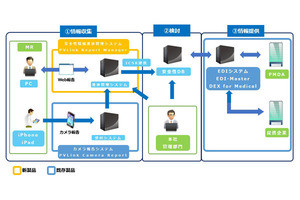
同社は、EDIシステム「EDI-Master DEX for Medical」を製薬企業向けソリューションとして提供しており、これまでPMDAに対する副作用報告の情報配信の仕組みとして、大手製薬企業80社以上の導入実績を持つ。今後、副作用報告についてトータルなソリューションを展開し、2022年までにPVLink Camera Reportの2018年度売上額に対し35%増を目指す考えだ。