大阪大学(阪大)と国立遺伝学研究所はこのほど、ゲノム編集技術「CRISPR/Cas システム」と「一本鎖オリゴ(ssODN)」を利用し、マウスやラットの遺伝子改変効率を向上させる新技術を開発したと発表した。
同成果は阪大大学院医学系研究科附属動物実験施設の真下知士 准教授、国立遺伝学研究所マウス開発研究室の吉見一人 助教らの研究グループによるもので、英科学誌「Nature Communications」に掲載された。
「CRISPR/Casシステム」は、DNAを切断する酵素Cas9と、ゲノム上の編集箇所を見つけ出すgRNAをマウスやラットなど動物の受精卵に注入することで、特定の遺伝子を破壊(ノックアウト)したり、特定の箇所へ導入(ノックイン)することができる技術。Cas9/gRNAと一緒に、ドナーDNA となる「ssODN」を導入すると、1~数十塩基(bp)のDNA配列をノックインすることができる。しかし、これまで動物の受精卵では、遺伝子などの大きなDNA配列の導入効率が低く、ノックイン動物を作製することが困難だった。
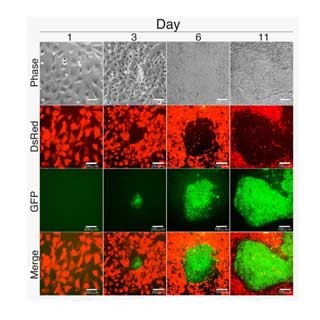
今回の研究では、受精卵でのCas9タンパク質の発現を上昇させ、ゲノム編集効率を向上することに成功したほか、1~3kbp程度の長い一本鎖オリゴを作製した。これらにより、GFP(緑色蛍光タンパク質)遺伝子の効率的かつ正確なノックインに加え、これまで不可能だった大きなサイズのゲノム領域(約200kbp)の導入、ラット遺伝子のヒト由来遺伝子への置き換え(遺伝子ヒト化動物)に成功した。
同研究グループは同成果について「マウスやラットなどのみならずさまざまな生物種における遺伝子改変操作の効率を向上させ、新しい遺伝子組み換え生物の作製に非常に有用な技術になることが期待されます。また、作製された遺伝子改変動物は、創薬研究、トランスレーショナル研究、再生医療研究などへの幅広い利用が期待されます。」とコメントしている。