産業技術総合研究所(産総研)は、光によって発熱できるカーボンナノチューブ(CNT)と特定の温度で内包分子を放出する温度感受性リポソームを組み合わせて、線虫Caenorhabditis elegans体内の細胞機能を制御できる分子複合体(ナノロボット)を開発したと発表した。
同成果は、産総研 ナノ材料研究部門の都英次郎 主任研究員らと、バイオメディカル研究部門の戸井基道 研究グループ長、大阪府立大学 大学院工学研究科の河野健司 教授らによるもの。詳細はドイツの化学誌「Angewandte Chemie International Edition」に掲載された。
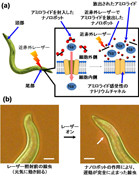
カーボンナノチューブ(CNT)は、そのまま水中に分散させようとすると、強い分子間の相互作用により束状や粒状に凝集してしまうが、今回の研究では、CNTの光発熱特性を最大限に利用し、かつ、リポソームと組み合わせて分子複合体を作製することを目的に、アビジンやポリエチレングリコール(PEG)、リン脂質(PL)から構成される分子(アビジン-PEG-PL)を単層CNTの表面にコーティングし、水中へ分散させ、温度感受性を与えたリポソームの自己組織化を利用しCNTとリポソームからなる分子複合体を作製したという。
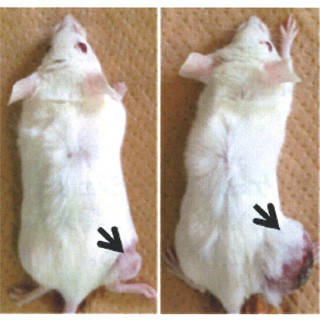
この分子複合体はナノスケールのロボットに例えられる「ナノロボット」に相当し、近赤外領域の光エネルギーを与えると内包している分子(薬物など)を放出し、この薬物により細胞機能を制御できることから、およそ1000個の細胞からなる線虫を対象にナノロボットの運動抑制効果の検証を行った結果、近赤外レーザー光を照射すると、線虫の動きが鈍化していき、最終的には停止することを確認したという。
また、細胞毒性と生体適合性を調べたところ、問題ないことが判明したほか、CNTの表面に結合したリポゾームが生体適合性を向上させることも明らかになったとする。
なお研究グループでは今後、今回の技術の応用として、生体組織のごく限られた領域だけに存在する細胞機能を個々に調べることで、がんや免疫疾患などの分子・細胞レベルでの病態解明につながる研究用ツールの開発を目指したいとするほか、生体内におけるナノ物質の健康面への影響は不明瞭な点もあるため、CNTを用いて作製するさまざまな物質の細胞毒性評価や生体適合性評価を進め、生体内で安心・安全に利用できる材料やシステムの開発を目指すとしている。