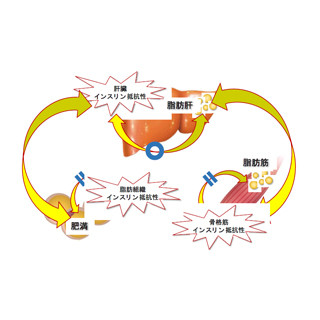
東京大学は4月3日、運動による脂質代謝改善に関わる新たな分子機構を明らかにしたと発表した。
成果は、東大大学院 農学生命科学研究科の佐藤隆一郎教授らの研究チームによるもの。研究の詳細な内容は、3月18日付けで「American Journal of Physiology Endocrinology and Metabolism」に掲載された。
メタボリックシンドロームの発症には、影響として運動習慣の有無が大きい。特に運動による脂質代謝改善においては、骨格筋で「リポタンパク質リパーゼ(LPL:Lipoprotein lipase)」発現が上昇することが重要だとされる。LPLは運動により発現上昇した後に血中に分泌され、「キロミクロン」や「VLDL」などのリポタンパク質中に含まれる「トリグリセリド」を分解。その後、分解産物である脂肪酸を骨格筋細胞が積極的に取り込むことで脂質代謝が改善する仕組みだ。しかし運動後の骨格筋でなぜLPL発現が上昇するのか、分子レベルで明確にはわかっていなかった。
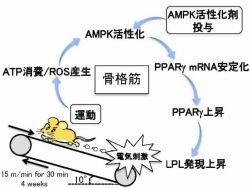
そうした中、近年、運動による代謝改善効果を担う因子として「エネルギーセンサタンパク質(AMPK:AMP-activated protein kinase)」が注目されている。AMPKは運動によって生じる細胞内エネルギー枯渇を感知し、その回復に努める機能分子だ。今回の研究では、AMPKが核内受容体「PPAR(peroxisome proliferator-activated receptor)γ1」の発現亢進を介してLPLの発現上昇を誘導することが新たに見出され、さらにAMPKによるPPARγ1の発現亢進の一部は、mRNAの安定化という一風変わった機構により調節されていることが明らかにされた(画像1・2)。
|

|
|
画像1(左):マウス骨格筋におけるLPL発現上昇の分子機構の概略図。ROS:活性酸素種(Reactive Oxygen Species)。画像2(右):骨格筋におけるLPL産生上昇の意義。CD36:細胞内へ脂肪酸を輸送する脂肪酸トランスポーター |
|
今回の研究では、斜度10°のトレッドミルを用い、マウスに対して毎分15mの速度で30分の走行運動を週5回、4週間にわたる負荷がかけられた。その結果、非運動群のマウスに比べ、運動群マウスでは骨格筋におけるPPARγ1およびLPLのメッセンジャーRNA(mRNA)量が有意に上昇することが認められたという。
核内受容体であるPPARファミリーはα、β/δ、γの3種類のサブタイプが存在し、さまざまなエネルギー代謝に関わることが知られている。骨格筋においてはPPARファミリー中のPPARα、およびPPARβ/δが脂肪酸代謝関連遺伝子の発現を調節する機能を持つ。一方、PPARγは脂肪細胞において重要な働きをしているが、骨格筋における発現量は脂肪組織の10%以下であることから、その機能については不明な点が多く残されていた。
そこで筋細胞におけるPPARγ1の機能を明らかにするため、培養筋管細胞「C2C12」にPPARγ1を過剰発現させ、種々の遺伝子発現応答の追跡が実施されたのである。その結果、LPL mRNAおよびタンパク質の突出した上昇が確認されたことから、PPARγ1がLPL発現を調節する因子であることが明らかになった。
さらに研究チームは、運動時にPPARγ1発現を上昇させる上流因子の同定を試みることにし、そこで着目した因子が運動により活性化するAMPKというわけだ。C2C12をAMPK活性化剤である「AICAR」や「メトフォルミン」、AMPKを間接的に活性化する「H2O2」を含む培地で培養すると、PPARγ1mRNAならびにタンパク質の上昇が確認された。この上昇は、同時にAMPK阻害剤を培地に加えると解除されたことから、AMPK活性化によりPPARγ1mRNAが上昇することが明らかになったのである。
さらにマウスに対して3日間にわたるAICARの投与が行われたところ、やはり骨格筋においてPPARγ1、LPL mRNAの有意な上昇が確認された。以上の結果より、運動→AMPK活性化→PPARγ1増加→LPL上昇の分子機構が明らかにされたのである。運動刺激により骨格筋はLPL分泌を上昇させ、エネルギー源となる遊離脂肪酸を細胞内に積極的に取り込む適応をしていると考えることができるという。
続いて、AMPK活性化によるPPARγ1発現上昇の分子機構の解析が行われた。その結果として興味深いことに、PPARγ1mRNAは通常およそ4時間の半減期で分解するのに対し、AMPKを活性化することで半減期が12時間程度まで延伸することが判明。ここで見られたmRNA安定化は、AMPK阻害剤により抑制された形だ。PPARγ1mRNAの「3'非翻訳領域」には、半減期の短いmRNAに特徴的な「AU-rich配列」が5カ所存在し、いずれもヒト、マウス、ラットで保存されている。この結果は、AMPKがAU-rich配列を介したmRNAの分解機構を抑制する作用を持つことを示唆しているという。
今回の成果により、骨格筋における、運動→AMPK活性化→PPARγ1増加→LPL上昇の分子機構が明らかとなった。AMPKは、運動のみならず食品に含まれる種々のポリフェノールなどによっても活性化されることが知られている。来るべき高齢社会において、運動が十分にできない高齢者の健康維持に、AMPK活性化能を持つ食品が活用されることが期待されるとした。