神戸大学は9月10日、近畿大学(近大)、大阪府立母子保健総合医療センター、奈良先端科学技術大学院大学(NAIST)、産業技術総合研究所(産総研)との共同研究により、腸管出血性大腸菌「O157」の病原タンパク質「EspB」のフレキシブルな全体構造の詳細を明らかにしたと発表した。
成果は、神戸大 医学研究科 構造生物学分野の濵田大三特命助教、近大医学部の坂田育弘教授、同・濵口満英助教、母子保健総合医療センター免疫部門の柳原格部長、NAISTの片岡幹雄教授、同・上久保裕生准教授、産総研の萩原義久主任研究員らの共同研究チームによるもの。研究の詳細な内容は、8月21日付けで米オンライン科学誌「PLoS ONE」に掲載された。
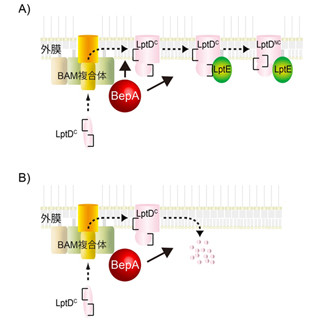
O157は複数の病原タンパク質を用いてヒトの腸管上皮細胞に強固に定着し、「ベロ毒素」を産出することにより、時には死に至るほどの重篤な症状を招く。O157が生産する病原タンパク質の1つであるEspBはヒトなどの宿主細胞の持つタンパク質「αカテニン」に結合することで、この「強固な定着」が起きる際に生ずるアクチン線維のバンドリングを促すタンパク質だ(画像1)。
EspBに関する先行研究により、その一部が緩く巻きあがった「αへリックス構造」という、部分構造を形成していることはすでに判明している。しかし、ほかの大部分が、フラフラとした立体構造を形成している「天然変性タンパク質」であるため、X線結晶構造解析や核磁気共鳴といった高分解能技術による詳細な立体構造解析が困難だった。
天然変性タンパク質とは、通常のタンパク質が密に詰まった堅い構造を形成するのに対して、広がった構造を持つタンパク質の総称だ。通常のタンパク質の構造がほどけて機能を喪失した状態である「変性状態」に相当する構造を天然の条件下で形成しているため、このような名前が付けられている。ただし天然変性タンパク質はほどけた構造のままでも、基本的な機能は保持されている形だ。
一般的に、ヒトを含む真核生物の遺伝子には天然変性タンパク質が30%程度含まれているのに対して、原核生物の場合は天然変性タンパク質は数%に満たないという。ただし、腸管出血性大腸菌を初めとする病原性の「グラム陰性菌」などの特殊なタンパク質分泌装置を持った細菌やウイルスの遺伝子上には、病原性に関わる天然変性タンパク質が比較的多くコードされていることが示唆されている。
そこで研究チームは今回、EspBを分断した断片を複数調製し、さまざまな分光学的・熱力学的研究手法を用いてその立体構造を解析し、これらの断片的な情報をパズルのピースとし、実際のジグソーパズルを解くようにそれらを組み合わせることで、フラフラとしたEspB全長の低分解能構造を明らかにした。
その結果、EspBの30番目~70番目のアミノ酸領域が、比較的安定でなおかつ伸びた状態のαへリックス構造を採っており、それ以外の領域は一時的にαへリックス構造を形成するものの、比較的ランダムな紐状構造を形成していることが示唆されたのである。さらに、30番目~70番目のαへリックス領域は、全長タンパク質と同程度の強さで、EspBの結合相手である宿主細胞由来のαカテニンと結合することでアクチン線維のバンドリングを促進することもわかったというわけだ。
今回の研究手法は、通常のタンパク質がアミノ酸配列上で遠距離にある原子間の相互作用によりしっかりとした立体構造を維持しているのに対して、天然変性タンパク質の場合、そのような遠距離の相互作用が存在しため、断片化を行っても、元の全長構造に近い構造を各断片が保持しているという、天然変性タンパク質に特有の性質が利用されている(画像2)。
今回の成果で得られたEspBの構造に関する知見は、O157による「強固な定着」の詳細なメカニズムの解明やEspBをターゲットとした治療薬の開発などに、今後、利用できるものと期待されるという。また、多くの細菌・ウイルス由来の病原タンパク質は、EspBと同様なフレキシブルな構造を形成しており、今回の研究で用いられた断片化による構造解析を根気よく進めることにより、これらの病原タンパク質の構造情報や関連する疾患の発症メカニズムの解明、治療薬の開発が、進むものと期待されるとしている。