奈良県立医科大学(奈良医大)は、京都大学、三重大学との共同研究により、一酸化窒素(NO)がパーキンソン病において活性が低下するタンパク質「parkin」を活性化させることで、パーキンソン病における細胞機能障害を防いでいることを突き止めたと発表した。
成果は、奈良医大 薬理学講座の小澤健太郎准教授、同・大学院生の小松原晃氏、同・川舟広徒氏、同・学部学生の辻優一氏、同・研究生の趙晶氏、同・京谷陽司助教、同・吉栖正典教授、京大大学院 医学研究科 臨床神経学 研究生の澤田知世氏、同・高橋良輔教授、三重大大学院 医学系研究科 薬理ゲノミクスの西村有平講師、同・田中利男教授らの研究チームによるもの。研究の詳細な内容は、7月16日付けで英オンライン総合学術誌「Scientific Reports」に掲載された。
パーキンソン病は加齢と共に発症し、手足のふるえ、手足のこわばり、動作が緩慢になったりするという症状が出る神経変成疾患の1種だ。パーキンソン病は神経伝達物質「ドーパミン」を作る神経細胞が減少することで発症すると考えられているが、その原因は未だに不明な点がある。
また近年の研究により、タンパク質parkinをコードする遺伝子に異常があると「常染色体性劣性遺伝性若年性パーキンソニズム」という家族性パーキンソン病(遺伝性のパーキンソン病)を発症することがわかってきた。parkinは異常なタンパク質を分解する働きがあり、この活性がなくなるとパーキンソン病を発症すると考えられている。しかし、パーキンソン病患者全体で見るとparkinに異常がある患者はごく一部であり、異常がない大部分の患者がなぜパーキンソン病を発症するのかは今もって解明されていない。
一方でNOは、ヒトの体の中で血管を弛緩させ、血圧を下げるという働きがあることがわかっている。この発見は1998年のノーベル生理学・医学賞の対象となり、現在ではNOを発生させるいわゆるニトロ製剤は狭心症の特効薬として広く使われている。このようにNOには血管において重要な役割を果たしているわけだが、その後の研究でNOはパーキンソン病の発症にも関係していることがわかってきた。しかしNOがどのようにパーキンソン病の発症に関わるのかは不明であり、またNOがパーキンソン病を治す方向に働くのか悪くする方向に働くのかも研究者によって異なる結果が出ているという状況である。
そこで今回、小澤准教授らの研究チームは、NOがparkinを修飾することによりparkinを活性化し、その結果、細胞機能障害を防いでいることを見出すことに成功した。さらに、NOはこの作用以外に細胞機能障害を増悪させる別のメカニズムが存在していることも証明したのである。
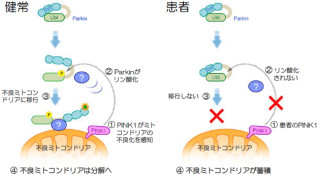
今回の研究では、まずNOを発生させる薬剤を添加し、NOがparkinを活性化させることを示した。実験では不要なタンパク質の「Tom20」をparkinが分解するのを確認し、そこにNOを加えると大幅に分解が促進されることが確かめられた形だ(画像1)。
次にparkinを構成するアミノ酸を人工的に1つだけ別のアミノ酸に置換する方法を用いて、parkinのどのアミノ酸がNOに修飾されているかを調査。すると、323番目のアミノ酸がNOに修飾されていることが発見されたのである。
次に、この変異parkinはNOにより活性化されないことが示され、このことより323番目のアミノ酸をNOが修飾することが、NOによるparkinの活性化のメカニズムであることを確認。この結果により、NOがどのようなメカニズムによりパーキンソン病の発症に関係しているのかが解明されたのである。
最後に長時間NOを添加し続けると、parkinの活性が低下してくることが示され、これはNOが「パーオキシナイトライト」という物質に変化することによるためであることも発見された。このparkinの不活性化は正常のparkinでも変異parkinでも確認されたことから、323番目のアミノ酸は直接関与していないことが判明。
この結果、NOはparkinの323番目のアミノ酸である「システイン」を修飾することでparkinを活性化させて細胞保護に働いているのに加え、パーオキシナイトライトに変化することでparkinを不活化し細胞機能障害を起こしていることがわかったのである(画像2)。
NOがパーキンソン病の発症に関わっていることは昔から示唆されていたが、そのメカニズムに関しては明らかではなく、今回の成果によってそのメカニズムの一端が明らかとなり、NOがパーキンソン病において発症を抑えるのと促進するのと両方に働いていることが解明された。このNOの2つの作用は異なるメカニズムによって起こっており、NOの細胞保護に働く作用だけを起こす薬を開発できれば、新しいパーキンソン病治療薬になることが期待されるとしている。