基礎生物学研究所(NIBB)は5月28日、緑藻が光合成の許容量を上回る過剰な光エネルギーを安全に消去するために、特殊なタンパク質を結合した巨大な光合成タンパク質超複合体「PSII-LHCII-LHCSR」を形成することが発見されたと発表した。
成果は、NIBB環境光生物学研究部門の得津隆太郎助教、同・皆川純教授らの研究チームによるもの。研究の詳細な内容は、米国東部時間5月27日付けで米国科学雑誌「米科学アカデミー紀要(PNAS)」に掲載された。
光合成反応の現場である植物や光合成藻類たちの葉緑体の中では、光の変化に応じて、さまざまな生物反応がダイナミックに展開されていることが明らかになってきた。中でも強い光、特に光合成の許容量を超えるような過剰な光から光合成の基幹部の「PSIIタンパク質複合体」を守るため、植物は余分な光エネルギーを安全に熱エネルギーに変換して消去する「qEクエンチング」反応を駆動することがわかっている。
しかし、このqEクエンチングがどこで、どのように行われているのか、これまで明確にした報告はなかった。そこで研究チームは今回、単細胞緑藻である「クラミドモナス」を用いて、qEクエンチング反応の実体解明を試みることにしたのである。
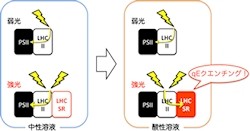
クラミドモナスの場合、qEクエンチング反応にはタンパク質「LHCSR」が深く関与すると考えられていた。今回の研究では、クラミドモナスに強い光を当て続け(画像1)、qEクエンチングを駆動している細胞から、その反応の実体をとらえることに成功した(画像2)。
それは、光合成反応の基幹部である、葉緑体中のチラコイド膜上に存在するタンパク質複合体「PSII-LHCII」にLHCSRが結合した「PSII-LHCII-LHCSR超複合体」だったのである。そしてqEクエンチングを引き起こすきっかけである「チラコイド膜内の酸性化」を模して、PSII-LHCII-LHCSRタンパク質超複合体を酸性溶液に入れたところ、照射した光エネルギーが消去されることが確認された。
今後は今回の技術を用いて、クラミドモナスだけではなく、地球上に繁栄している陸上の高等植物や水中のさまざまな光合成藻類が、どのようなqEクエンチング装置を備えているのかを明らかにし、強光防御装置の進化を解き明かすことが可能になるだろうと研究グループは説明する。
また、qEクエンチング超複合体の詳細な解析を進めることで、光エネルギーの消去、つまりエネルギー損失の過程を明らかにし、より効率的に光エネルギーを利用可能な光合成生物の創成につながるものと期待されるとしている。