大阪大学(阪大)は5月13日、名古屋大学(名大)との共同研究により、細胞と細胞をすき間なくつなげるタンパク質である「クローディンファミリー様タンパク質」の分子構造を解明し、細胞間接着装置が持つ複雑な機能の解明に向けて重要な知見を得ることに成功したと発表した。
成果は、阪大大学院 生命機能研究科・医学系研究科の月田早智子教授、名大 細胞生理学研究センター(CeSPI)の藤吉好則教授らの共同研究チームによるもの。研究の詳細な内容は、4月23日付けで英国科学誌「Nature Communications」に掲載された。
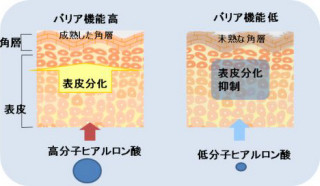
ヒトは体内と外界を隔てることで身体の恒常性を維持しているのが、その隔てる役割を担っているのが、いわずと知れた表皮をはじめとする「上皮組織」だ。上皮組織は隣り合う細胞と細胞がしっかりとつながり合うことで細胞のシートを形成している。そして、そのつなぎ合う機能を果たしているのが細胞間接着装置だ。中でも構造体「タイトジャンクション(Tight junctions:TJs)」は、タンパク質「クローディン」により細胞と細胞の距離をほぼ0にまで近づけ、体内と外界を隔てることに寄与していることが知られている。
クローディンは、細胞間接着部位において膜平面内で線状に重合(「ストランド形成」)して上皮細胞間バリアを構築している形だ。よって、TJsからストランドが消失すると細胞間バリア機能がなくなってしまう。クローディンはヒトやマウスでは、現在27種類のサブタイプが確認されており、サブタイプ特異的な細胞間バリア機能やストランドの形態(平行型もしくは分岐型)が存在すると考えられる。つまり、臓器特異的に発現するクローディンが、細胞間にストランドを作ることこそが、適切なバリア機能の形成に必須だと考えられているのである。
しかし、クローディンは如何にして細胞膜(脂質二重層)という2次元平面の場所で、線状に重合するのか、そこにはどのような分子間相互作用が働いているのかはわかっていない。また、立体構造もいまのところは不明だったが、研究チームは今回の研究を経て、分子量29kDaの小さな4回膜貫通タンパク質「IP39」によって脂質平面内におけるTJ-ストランド形成原理モデルの1つを構造学的に提示することに成功した。
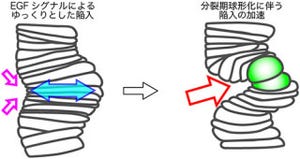
膜タンパク質が脂質膜のような2次元平面内で相互作用することで重合鎖を作る際、その結合による歪みから、重合は直線状ではなく湾曲することで、次第にはリング状の分子鎖が構成されていく。しかし、IP39は4つの分子間相互作用を持つことで湾曲することを抑制し、直線状の重合鎖形成を可能としていると考えられた。2次元結晶化されたIP39の構造は、細胞骨格タンパク質の存在なしにIP39単独で直線状に重合できることを意味しており、分子量29kDaの小さな4回膜貫通タンパク質がこのような平面内配向を見せる例は過去に例がない。
将来的にクローディンの構造が解明される時、今回の研究はクローディンの機能および構造解析において重要な知見、テンプレートとなるという。さらに組織特異的に発現しているクローディンのバリア機能の解析につながり、「クローン病」などの細胞間接着不全による炎症性腸疾患のようなクローディンとの関連が報告されている疾患においても、新規治療薬の設計において大きな知見につながる可能性があるとしている。