理化学研究所(理研)は、Ca2+シグナルにより脳内の神経伝達と血管収縮の調節を行う細胞「アストロサイト」が、放射状に伸びる突起部分だけにより多くCa2+シグナルを発生させることを突き止め、各々の突起が独立して働く仕組みの一端を発見したことを発表した。同成果は、理研脳科学総合研究センター発生神経生物研究チームの御子柴克彦チームリーダー、有薗美沙ジュニア・リサーチ・アソシエイト、坂内博子研究員らによるもので、米国の科学雑誌「Science Signaling」に米国時間4月3日に掲載される予定であるほか、同雑誌に掲載される論文のなかから面白いトピックスを紹介するScience Signaling podcastにおいて4月15日頃から公開される予定だ。
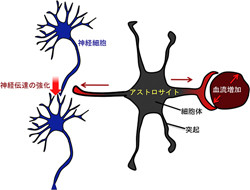
脳は神経細胞とグリア細胞、血管で構成されており、グリア細胞の一種であるアストロサイトは、これまで神経細胞が働く環境を整える黒子のような存在として認識されてきた。しかし近年の研究により、アストロサイトがCa2+シグナルを用いて周辺の細胞に情報伝達することで神経伝達や神経細胞に養分を送る血流を調節していることが明らかとなり、脳機能の調節に積極的に関わる役割を担う重要な役者として注目されるようになってきた。
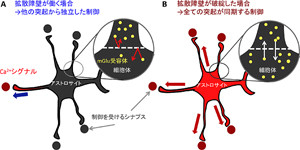
アストロサイトは、遺伝情報を含む核がある細胞体と、それをとりまく複数の突起で構成されており、これらの突起は独立して働き、神経細胞のシナプスを覆ったり、血管に巻きついたりしている。神経細胞からの入力などでアストロサイト内のCa2+濃度が上昇すると、Ca2+シグナルが生じて、神経伝達を強化したり血流を増やすことで神経細胞へ送る養分を増加させたりする。
アルツハイマー病やてんかんなどの脳疾患では、複数のアストロサイト間を横断するCa2+シグナルや、アストロサイトの細胞体での頻繁なCa2+シグナルが観察されている。健康な脳には見られないこうした異常に活発なアストロサイトのCa2+シグナルの原因は、それぞれの突起の独立した働きが何らかによって妨げられ、複数の突起の活動が同調することで起きる可能性があるとされている。これはつまり健康な脳には、アストロサイトの突起がそれぞれ独立して働けるようにCa2+シグナルの発生する場所を正しく調節する機構が存在することを示唆したものであるが、これまでは技術的な理由から細胞体のCa2+シグナルだけしか観察できなかったため、1つのアストロサイトがどのようにCa2+シグナルの空間的広がりをコントロールするかはまったく不明で、なぜ1つの細胞体から伸びる複数の突起が独立に働くことができるのかは分かっていなかった。そこで今回の研究では、1つのアストロサイトの突起がそれぞれ独立に神経伝達や血流を調節できる機構の解明に向けた取り組みが行われた。
研究チームでは、神経伝達と血管の調節に重要なCa2+シグナルを発生させる代謝型グルタミン酸受容体(mGluR)に注目し、1つの細胞の詳細なCa2+シグナルを観察できるように、Ca2+の濃度変化を蛍光強度で示すことができるCa2+センサのGCaMP2を用いた実験手法を確立した。
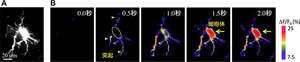
これをラットの海馬から培養されたアストロサイトに導入したところ、アストロサイトの細胞体だけでなく突起にいたるまで詳細なCa2+シグナルを観察できることが確認された。同手法を用いて同様に培養されたアストロサイト全体のmGluRを同時に活性化させたところ、ほぼすべての細胞でこれまで見過ごされていた突起部分からCa2+シグナルが始まることが見いだされ、これは、アストロサイトがそれぞれの突起の独立性を保つために重要な性質であると考えられるという。
|
|
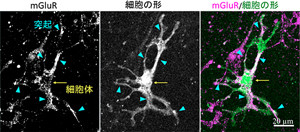
図2 突起から始まるアストロサイトのCa2+シグナル。 |
次に突起からCa2+シグナルが始まりやすい理由を調べるために、mGluRの分布を免疫染色法で調べた結果、mGluRが突起部分に多く存在していることが判明した。
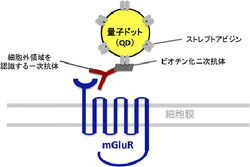
通常、細胞膜には流動性があり、膜分子は膜上を自由に動くことができるはずであることから、mGluRが突起に集まった状態を維持できる仕組みを明らかにするために、mGluRを量子ドットで標識し、その動きの追跡を行った。
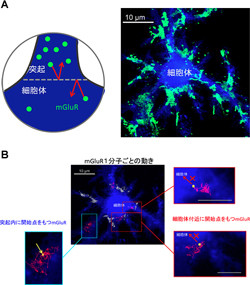
結果、mGluRは細胞膜上を動くことはできるものの突起と細胞体の間をまったく移動できないことが判明した。突起の真ん中にあるmGluRは、さまざまな方向に動けるが、細胞体付近にある場合は細胞体側へは動けなかったという。
つまり、突起と細胞体の間にmGluRに対する拡散障壁があることがこれにより判明したほか、mGluRの細胞内領域を強制的に発現することで拡散障壁を乗り越える環境を作り出し、人為的にmGluRが突起と細胞体の間を行き来できるようにした場合、mGluRはアストロサイト全体に均一に分布し、アルツハイマー病やてんかんなどの脳疾患で観察されたように細胞体からもCa2+シグナルが生じやすくなることも確認された。
これらのことから、アストロサイトはmGluRに対する拡散障壁を突起と細胞体の間に設けることで、突起部分に集中するmGluRを維持してCa2+シグナルを発生させやすくしていることが判明した。
この発見は、アストロサイトの突起が拡散障壁という「仕切り」によって機能的に独立しているというまったく新しい概念を示したものであるほか、アルツハイマー病やてんかんなどの脳疾患のアストロサイトでは拡散障壁が働いていない可能性を示した点でも大きな意義があり、これらの脳疾患ではアストロサイトの突起ごとの「仕切り」が機能しなくなり、複数の突起の働きが同調して症状を悪化させていると考えられると研究グループでは説明している。
脳機能を正常に維持するためには周辺細胞との情報伝達が重要であるが、今回の研究成果から、脳機能の秩序を保つアストロサイトの存在が疾患克服のための重要な因子であることが示唆されることから、今後は、アストロサイトCa2+シグナルが脳疾患研究の新しいターゲットになることが期待できるという。