京都大学(京大)は2月20日、フランスを中心とする欧州のゲノム解析センターと共同で、脂肪酸センサ分子の肥満患者におけるゲノム解析研究を行い、脂肪センサ「GPR120受容体」が食事性肥満の原因遺伝子であることを見出したと発表した。成果は京都大学薬学研究科の辻本豪三教授、同平澤明准教授、同市村敦彦大学院生(現 東北大学大学院医学研究科助教)らの研究グループによるもので、論文は英科学雑誌「Nature」オンライン速報版に英国時間2月19日に掲載された。
現在、肥満および肥満に随伴するあまざまな代謝異常(脂肪肝、糖尿病など)が世界的な健康問題となっている。この世界的な肥満大流行は、特に先進国の食生活がカロリー過剰摂取となりがちな高脂肪食であることに起因している。また、この食事性肥満には大きく遺伝的要因が関連することが考えられていたが、今までそのような原因遺伝子は見つかっていなかった。
そこで研究グループでは、2005年にヒトゲノムデータベースにより発見されていたGRP120受容体に着目。同受容体を欠損するマウスモデルを作出し、同受容体の生理機能の解析が行われた。
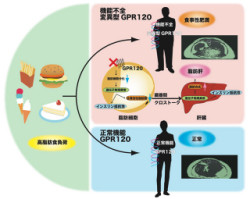
具体的には、「遺伝子改変マウスでの肥満、代謝疾患(逆遺伝学研究)」が1つ。GPR120遺伝子を欠損したマウスは高脂肪食負荷により肥満、糖尿病、脂肪肝の代謝異常を発症した。さらに、その種々の代謝異常は、GPR120遺伝子を欠損した脂肪組織ではその分化が遅延し、さらに脂肪酸合成の低下をきたすことによることを明らかにした。
2つ目は、ヒトでの肥満との関連(前向き遺伝学研究)。ヒトのGPR120のアミノ酸配列に1カ所変異が入った変異受容体では、センサ機能に異常が起こることを見出したのである。欧州の約2万人の肥満患者の遺伝子解析より、この変異を有するヒトでは、(特に欧州の高脂肪食環境下では)食事性肥満を発症する可能性が高いことが明らかにされた。
今回の成果は、GPR120が食事性の肥満に強く関与することを示している。今後、肥満や糖尿病に代表される代謝疾患に対して、GPR120を標的とした予防・治療薬への応用の可能性が期待されるとした。