次に、p3-Alcβの37アミノ酸の中から機能部位を決定するため、断片化したペプチドを用いた検証が行われた。すると、9~19番目の11アミノ酸(p3-Alcβ9-19)がその機能部位であると判明。p3-Alcβ9-19は、p3-Alcβ37と同様に有意に神経細胞のミトコンドリアを活性化させ、Aβオリゴマーに起因する傷害から神経細胞を保護する作用を有することが見出された。
Aβオリゴマーは細胞内への過剰なカルシウムイオンの流入を引き起こし、それが神経変性の引き金となることが報告されている。そこで、p3-AlcβがAβオリゴマーによる毒性から神経細胞を保護する仕組みを調べるため、同イオンが着目された。そして解析の結果、p3-Alcβ9-19とp3-Alcβ37は、AβオリゴマーによるNMDA型グルタミン酸受容体(GluR)の異常活性化を介したカルシウムの過剰な流入を抑制していることが解明されたとする。
-

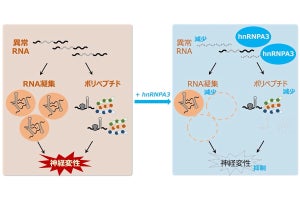
(左)p3-Alcβの産生機構。p3-AlcβはAlcβから、AβはAPPから切断酵素による切断を受けて細胞外に分泌される。(中央・右)p3-Alcβの作用機構。(中央)Aβオリゴマーが、NMDA型GluRを非生理的に活性化し、異常なカルシウム流入を引き起こすことで、ミトコンドリアの機能低下と神経細胞死を誘発する。(右)p3-Alcβは、NMDA型GluRの異常活性化を抑制し、Aβオリゴマーによるミトコンドリアの機能低下を防ぎ、神経細胞を健常な状態へ回復する。p3-Alcβが加齢およびADの進行に伴い減少することが確認されている(出所:北大プレスリリースPDF)
脳を含む中枢神経に作用する薬剤は血液脳関門(BBB)によって、投与しても作用部位へ十分な量を到達させられないことが大きな課題だ。しかし、p3-Alcβ9-19を末梢投与したラットでは、PETを用いた脳画像解析で脳のミトコンドリア活性が上昇。p3-Alcβ9-19が中枢神経系に到達し、末梢投与でもBBBを透過して機能を発揮することが確認された。
また、ヒト型の神経毒性を示すAβを産生しない野生型マウスと比較して、低下していたADマウスモデルのミトコンドリアの活性が、p3-Alcβの投与によって野生型のレベルにまで回復。そのことから、個体レベルでもp3-Alcβが、Aβオリゴマーによる神経毒性から神経機能を保護することが示されたとする。
-

p3-AlcβのAD治療薬としての活用。AD初期患者ではp3-Alcβの低下が認められる。有意な記憶障害が生じる時期からp3-Alcβ(経皮吸収剤名ALC919)を投与することで、ADの進行を遅らせ認知機能障害を抑制する効果が期待できる(出所:北大プレスリリースPDF)
研究チームによると、今回の研究からp3-AlcβがADに有効であることが示唆され、ADに有効な新規治療法につながる可能性があるという。同研究チームは現在、米・パスポートテクノロジーと共同で、マイクロポレーション装置を用いたp3-Alcβ9-19の経皮吸収製剤「ALC919」を開発中で、今後臨床試験を実施する予定としている。