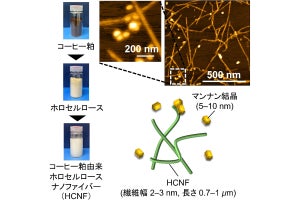
九州大学(九大)は7月24日、木とヒトに共通するナノ構造である「ナノファイバー形状」と「規則的な多糖界面構造」に着目し、本来細胞接着の能力をまったく持たない樹木由来の「セルロースナノファイバー」(CNF)に、結晶構造を保ったまま硫酸基などの生体官能基を導入することで、すぐれた細胞接着性と増殖性が発現することを発見したと発表した。
同成果は、九大大学院 生物資源環境科学府の甲斐理智大学院生、同・大学大学院 農学研究院の畠山真由美助教、同・北岡卓也教授、横河電機の岩本伸一朗博士らの共同研究チームによるもの。詳細は、糖質科学に関する全般を扱う学術誌「Carbohydrate Polymers」に掲載された。
ヒトは表皮細胞などの一部を除けば、再生できない細胞が多いため、疾患や負傷などによって組織や臓器などが機能を失った場合、それが致命的な場合は臓器移植に頼るしかないのが現状だ。そうした中iPS細胞などを用いて、組織や臓器を細胞から修復・再生する再生医療の研究が進んでいる。
再生医療に用いられる細胞の多くは、患者本人やドナーから採取した後、身体の外で培養・増殖させた後に使用する。一般的な細胞培養では、培養液にウシの血清を添加したり、細胞が接着するための足場として動物由来のコラーゲンが使用されたりしている。
しかし、再生医療の現場で使用する場合、動物由来素材には免疫拒絶や感染症のリスクがあるため、動物由来成分フリー(ゼノフリー)な培養環境が強く求められている。ゼノフリーな培養液がさまざまなメーカーで開発されている一方で、細胞が育つ足場材料には依然として動物由来材料が用いられている状況が大きな課題だという。
そこで研究チームは今回、培養液と足場の両方をゼノフリーな環境にするため、樹木由来のCNFを用いて細胞培養足場を作製し、成体内に存在、骨や軟骨、脂肪、筋肉などさまざまな細胞へと分化できる細胞である「間葉系幹細胞」を培養することにしたという。
ヒトの体内では、タンパク質の「細胞外マトリックス」と多糖の複合体が細胞の足場となっており、主要成分には線維状のタンパク質である「コラーゲン」や、酸性多糖の「ヒアルロン酸」などが知られている。研究チームは今回、多糖で構成されているCNFの表面を化学修飾することで、細胞外マトリックス成分に見られる線維形状と糖鎖構造の両方の特徴を備えた足場を作製できると考察。生体多糖の官能基に着目し、硫酸基で修飾した「硫酸化CNF」(S-CNF)と、カルボキシ基で修飾した「TOCNF」を用いて足場を作製することにしたという。
まず、修飾度合いの異なるS-CNF(横河電機製)と、繊維の長さが異なるTOCNF(日本製紙製)を組み合わせて、動物成分を含んだ培養液中で"不死化した"間葉系幹細胞が良好に育つ条件が検討された。なお、正常な細胞は細胞分裂を無限に繰り返すことができず、分裂回数には限界がある。そこで、細胞不死化酵素の「テロメラーゼ」などを導入して、無限に細胞分裂ができるようにしたものが不死化細胞であり、実験細胞として研究において使用されている。その後、ゼノフリーな培養液を使用して、間葉系幹細胞の増殖性が確認された。すると、従来の足場材料に使われてきた動物由来のコラーゲンに匹敵する増殖性をCNF足場で発現させることに成功したという。
しかし、遺伝子組み換えした不死化間葉系幹細胞では、再生医療に用いることはできない。そこで、再生医療への応用に向けて、ヒトから採取した「初代細胞」(生体組織から採取したそのままの細胞のこと)の間葉系幹細胞を用いて、ゼノフリー培養が行われた。すると、不死化した間葉系幹細胞と比べて細胞が増殖しにくい初代細胞の間葉系幹細胞においても、表面改質CNF足場では良好な細胞増殖性が示されたとする。
一方、汎用のプラスチック足場では、不死化間葉系幹細胞では良好に増殖していたものの、初代培養では増殖性が著しく低下することが確認された。つまり、ヒト幹細胞培養において、樹木由来CNFが優れた素材であることが明らかにされたのである。
研究チームは今後、表面改質CNF足場上で培養した初代間葉系幹細胞の特性解析や、細胞が分泌する有効成分の解析などを行うことで、再生医療や創薬支援基盤技術への応用を目指すとしている。