実験動物中央研究所(実中研)と慶應義塾大学(慶大)は7月1日、ゲノム編集により先天性免疫不全の霊長類の作出に成功したと発表した。
同成果は、実中研 マーモセット研究部 佐々木えりか部長(慶大先導研究センター特任教授)と慶大医学部生理学教室 岡野栄之教授らの研究グループによるもので、6月30日付けの米国科学誌「Cell Stem Cell」に掲載された。
同研究グループは2009年に、小型で繁殖力の高い霊長類「コモンマーモセット」を用いて世界初のトランスジェニックマーモセットの作製に成功していた。しかし、多くのヒト疾患モデルマウスが作製されてきた標的遺伝子ノックアウト技術はマーモセットを含む霊長類にはこれまで適用できていなかった。
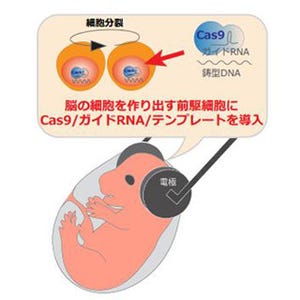
今回、同研究グループは、免疫不全マーモセットを作出するため、標的となるマーモセット受精卵のIL2rg遺伝子に特異的に結合して切断する人工ヌクレアーゼ(Zinc Finger NucleaseまたはTALEN)を作製。これを、体外受精させた前核期の受精卵に注入した後、この胚でゲノム編集がなされているかについて解析する手法を開発した。
同手法は、作製したゲノム編集の人工ヌクレアーゼが目的の遺伝子のゲノム編集を行い、さらにゲノム編集された遺伝子を持って生まれてくる新生仔がゲノム編集前と異なる形質を持つかどうかを予測できるもので、マウスよりも妊娠期間が長い霊長類で、ゲノム編集に失敗した新生仔を極力減らすことにより、研究を迅速に進めることが可能となる。
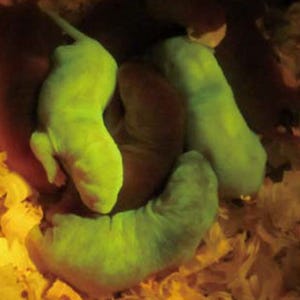
さらに同研究グループは、同手法によって評価された人工ヌクレアーゼを導入したマーモセット受精卵を数日間培養し、正常に発生している受精卵のみを仮親の子宮に移植した。この結果、3頭の免疫不全マーモセットが作出され、1年以上経過した現在もクリーン飼育室内で元気に生育しているという。
同マーモセットは、新生児期には免疫細胞の一種であるT細胞がほとんど欠落していたが、生後半年を超えるとT細胞の増殖が認められた。この現象は特定のヒトの重症複合型免疫不全症の病態を反映するものであり、同研究グループは、今後のヒト免疫不全症治療法開発のモデル動物として注目されるほか、iPS細胞を用いた臓器再生医療の治療法開発における有効性・安全性の検証研究にも有用なモデルであるとしている。
また、今回開発された人工ヌクレアーゼの機能評価方法は、今後多くの標的遺伝子ノックアウトモデルを作製するうえで有効な方法であり、この方法の応用によりヒト自閉症や統合失調症などのマーモセットによる精神神経疾患モデルの開発が期待されるという。