ナノ医療イノベーションセンター(iCONM)は5月17日、がん内部の微小環境で、治療抵抗性を持つ悪性度の高いがん細胞が存在する「腫瘍内低酸素領域」を、高感度でMRIにより可視化できるナノマシン造影剤を開発したと発表した。
同成果は、ナノ医療イノベーションセンター 米鵬 主任研究員、片岡一則 センター長(東京大学政策ビジョン研究センター・特任教授)、東京工業大学科学技術創成研究院 西山伸宏 教授(ナノ医療イノベーションセンター主幹研究員)、放射線医学総合研究所 青木伊知男 チームリーダーらの研究グループによるもので、5月16日付けの英国科学誌「Nature Nanotechnology」に掲載された。
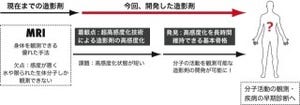
これまでがんのMRI診断においては、がんの悪性度がわからない、感度があまり良くないなどといった課題があったが、片岡センター長は、今回開発されたナノマシン造影剤について、「MRIでの検出が不可能とされていた非常に小さな転移がんを見つけられることがわかった。また、がんの悪性度をMRIで調べることができるというのがポイント。広く普及している安価な1テスラの低磁場MRIを利用するもので、医療費を上げずに性能を上げることができる造影剤」であると説明している。
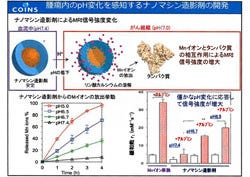
同研究グループが今回開発したナノマシン造影剤は、がん組織内の低pH環境に応答して溶解する性質を持つ「リン酸カルシウムナノ粒子」に、MRI造影効果を有するマンガン(Mn)造影剤を搭載したもの。同造影剤を内包した内核が、生体適合性に優れたポリエチレングリコールの外殻で覆われており、粒径は60nm程度となっている。西山教授によると、「これらの成分はすべてFDA(米国食品医薬品局)から承認を受けている材料なので安全」であるという。
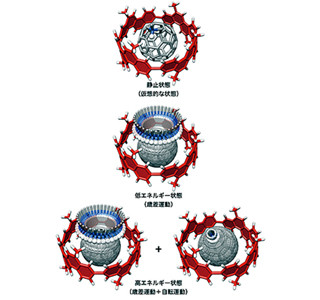
pH7.4という血流中の環境では安定に存在する同造影剤だが、pH6.5~6.7という低pHとなる腫瘍内の環境においては、pHに応じてリン酸カルシウムが溶解し、Mnイオンが放出される。そしてこのMnイオンが、がん組織中のタンパク質と相互作用することによって、がん組織選択的にMRI信号強度が増大するという仕組みになっている。
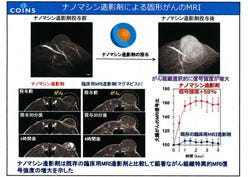
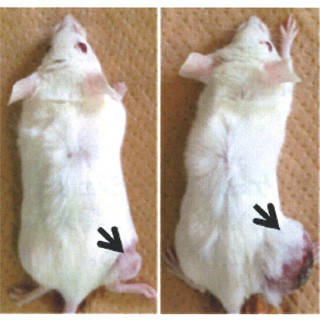
同造影剤をがん細胞の皮下移植モデルマウスに投与し、MRI計測を行った結果、投与30分で腫瘍全体を造影することができ、また時間の経過とともに腫瘍中心部の信号強度が増大することが確認されている。このMRI信号強度の変化は、既存の臨床用MRI造影剤「マグネビスト」による信号強度変化よりも約60%程度大きいものであったという。
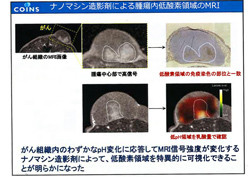
また、腫瘍中心部で信号が顕著に増大する部分は、組織切片の免疫染色の結果から、がんの「低酸素領域(Hypoxia)」と一致していることがわかった。これに加え、がんの内部で乳酸が溜まる部位とも一致しており、低酸素領域を特異的に可視化できることが明らかになっている。
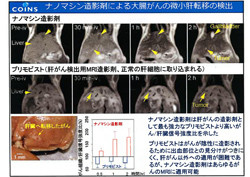
さらに、同造影剤を1.5mmの小さな大腸がんの肝転移モデルにおいてMRIで計測した結果、既存の肝がん用MRI造影剤「プリモビスト」よりも優れた検出力を示すことがわかっている。また、プリモビストはがんが陰性に造影されるために、出血部位との見分けがつきにくく、肝がん以外への適用が困難であったが、ナノマシン造影剤では、あらゆるがんに適用が可能だという。
がんの低酸素領域には、抗がん剤治療や放射線治療に対して抵抗性を示す悪性度の高いがん細胞が潜むことが知られており、がんの内部に低酸素領域を持つかどうかを調べることは、治療方針の決定や治療効果の検証に重要であるといえる。
「微小転移がんの検出や、コンパニオン診断薬(ナノマシン治療の効果を予測するもの)など、ナノマシン造影剤はがん治療と組み合わせることでさまざまな使い方が考えられる。抗がん剤を搭載したナノマシンの臨床試験はすでに第3相まで進んでおり、どういう風に臨床試験に展開していくかという戦略が、なるべく早く患者さんにお届けするのに重要となってくる。これについては企業やドクターの方々と相談しながら進めていきたい」(西山教授)
同成果については、すでにいくつかの企業から引き合いがあるといい、同研究グループは、数年以内にも同造影剤の実用化を目指していきたい考えを示している。