基礎生物学研究所(NIBB)は7月1日、記憶、神経変性疾患、ストレス防御などに関わるRNA粒子の集合・離散を制御する新たな仕組みを解明したと発表した。
同成果は、NIBB(岡崎統合バイオサイエンスセンター) 神経細胞生物学研究室の椎名伸之 准教授、同 中山啓 助教らによるもの。詳細は米国の科学専門誌「Journal of Biological Chemistry」(先行電子版)に掲載された。
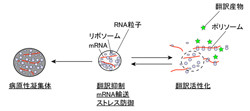
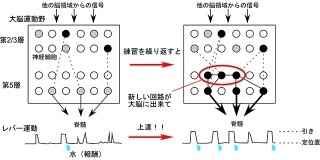
近年の研究から、細胞内に存在するRNA粒子の集合や離散が正しく起こることがウイルス感染や酸化ストレスに対する細胞の防御機構に必要であり、特に神経細胞では記憶の形成にも必要なこと、ならびに集合・離散の異常が、筋萎縮性側索硬化症(ALS)や前頭側頭葉変性症(FTLD)などの神経変性疾患の発症と密接に関係することなどが分かってきた。
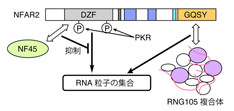
今回の研究では、これまで同研究グループが報告してきたRNA粒子の構成要素であるRNA結合タンパク質「RNG105」の結合因子を網羅的に同定し、その中からRNA粒子の集合・離散を調節する因子を見出すことを試みたという。
その結果、ウイルスRNAやmRNAの翻訳を抑制し、ウイルス感染に対する防御機能をもつ2本鎖RNA結合タンパク質「NFAR2」がRNA粒子の集合を促進すること、逆にNFAR2の結合タンパク質「NF45」がRNA粒子の離散を促進することを発見したという。
また、NF45を恒常的に過剰発現させた細胞では、通常酸化ストレスによって促進されるRNA粒子の集合が阻害され、それに伴い、細胞がストレスに対して脆弱になるという結果も得たとのことで、これにより、NFAR2とNF45によるRNA粒子の集合・離散制御が、RNA粒子の機能に重要な役割を担うことが示唆されたとする。
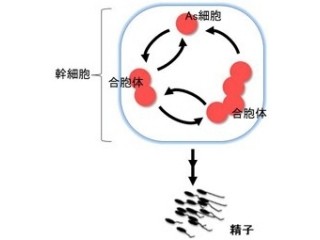
なお研究グループでは今後も、神経細胞でのRNA粒子の役割に注目し、NFAR2やNF45が記憶・学習においてどのような役割を担うか、ならびに、NFAR2やNF45の機能異常が神経変性疾患とどのような関係があるかの解明を進めていくことで、RNA粒子の異常と神経変性疾患の関連性についての共通原理を解明していきたいとコメントしている。