東北大学は4月22日、メラニン合成酵素を細胞内小器官「メラノソーム」に受け渡す過程を制御する分子複合体を同定したと発表した。
成果は、東北大大学院 生命科学研究科修士大学院生の谷津彩香氏、同・福田光則教授らの研究チームによるもの。研究の詳細な内容は、現地時間4月2日付けで米国の皮膚科学専門雑誌「Journal of Investigative Dermatology」電子版に掲載された。
ヒトの肌や髪の毛に含まれる黒いメラニン色素は、有害な紫外線から体を守るために重要な役割を果たしているが、その一方で、しみやそばかすの原因ともなっており、特に女性にとってはやっかいな存在にもなっている。
メラニン色素は、特殊な細胞の「メラノサイト」に存在するメラノソームの中で、膜タンパク質(細胞膜などに刺さった形のタンパク質)の「メラニン合成酵素」により、アミノ酸「チロシン」から複雑な酵素反応のステップを経て合成され、貯蔵される形だ。
メラノソームはオルガネラ(細胞内小器官)の1つで袋状(小胞)をしており、メラニン色素の合成・貯蔵に特化している。このメラノソームは、メラノサイトの細胞内を、「微小管」と「アクチン線維」という細胞内骨格でできた"道路"に沿って細胞膜近傍まで輸送され、肌や髪の毛を作る細胞に受け渡されて初めて、肌や髪の毛の暗色化が起こるのだ。
またメラニン合成酵素には、「チロシナーゼ(Tyr)」、「チロシナーゼ関連タンパク質1(Tyrp1)」、「チロシナーゼ関連タンパク質2(Trp2/Dct)」の3種類があり、今回の研究では主にType1に焦点が当てられた。
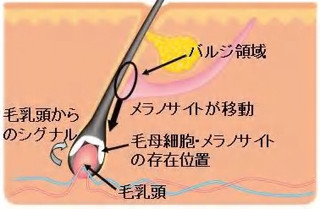
なお、メラニン合成酵素ははじめからメラノソームに存在するわけではなく、Tyrp1の場合はオルガネラの1つである「小胞体」で合成されて、同じく「ゴルジ体」で糖鎖修飾を受けた後、交通整理人役のタンパク質複合体「Rab32/38.Varp複合体」に助けられる形で、「小胞輸送」(細胞質に拡散しないよう小胞体に乗った形で輸送される過程のこと)により未成熟なメラノソームに輸送される(画像1・ステップ1)。その後、メラノソームへと受け渡されたメラニン合成酵素は(画像1・ステップ2)、メラノソームの中でメラニン色素を合成し(画像1・ステップ3)、黒い成熟したメラノソームになるというわけだ。
つまり、メラニン色素を正しく合成するためには、メラニン合成酵素をメラノソームに輸送するプロセスが重要というわけだ。実際、ヒトの「TYR遺伝子」や「TYRP1遺伝子」などが変異するとのメラニン合成酵素の輸送に異常が起こり、肌や髪の毛が白くなる(色素の欠乏状態が起きる)「眼皮膚白皮症I型」や同「III型」、「ヘルマンスキー・パドラック症候群」などを発症することが知られている。
これまで、メラニン合成酵素の輸送に関わるRab32/38.Varpなどの分子群の存在は確認されているが、実は小胞に乗って運ばれてきたメラニン合成酵素がメラノソームの袋にどのように受け渡されるのか(画像1・ステップ2)はよくわかっていなかった。それが今回の研究で、解明されたのである。
研究チームは今回、メラニン合成酵素がメラノソームに受け渡される過程に「膜融合」が関与するのではないかと考察。そして、膜の融合装置の実体と考えられている「SNARE(soluble N-ethylmaleimide sensitive fusion protein attachment protein receptor)タンパク質複合体」に着目した。
一般的に、SNAREタンパク質複合体による膜融合は、輸送されて来た小胞上に存在する1種類の「v-SNARE(vesicleSNARE、小胞側のスネアの意味)」と受け手側の膜に存在する2種類の「t-SNARE(targetSNARE、ターゲット側のSNAREの意味)」が、カギとカギ穴のような関係で結合することにより引き起こされる(画像2)。
研究チームのこれまでの研究により、メラニン合成酵素のTyrp1を含む小胞上に「Varp結合分子」として、v-SNAREの1種である「VAMP7(vesicle-associated membrane protein 7)」が存在することを見出していたが、その詳細な機能までは明らかにしていなかった。そこで今回の研究ではまず、VAMP7の相方となるメラノソーム上の2種類のt-SNAREを探索。その結果、「シンタキシン3」と「SNAP23」を見出すことに成功したのである。
次に、3種類のSNAREタンパク質、シンタキシン3、SNAP23、VAMP7の細胞内局在、および内在性分子のノックダウンによるメラニン合成酵素の発現・分布に対する影響が検討された(画像3・4)。

|

|
|
SNAREタンパク質ノックダウン細胞におけるメラニン合成酵素の消失の様子。RNA干渉法によりSNAREタンパク質(シンタキシン3、VAMP7、SNAP23)のいずれかをノックダウンしたメラノサイト(白い波線の細胞)では、メラニン合成酵素Tyrp1およびチロシナーゼのシグナルが顕著に減少する。画像7(左)はTyrp1、画像8はチロシナーゼのもの。スケールバー=20μm |
|
検討の結果により、以下の4点が明らかにされた。
1.マウスの培養メラノサイト(melan-a細胞)においては、t-SNAREの候補としてシンタキシン3とSNAP23が内在性に発現しており(画像3)、これら2種類のt-SNAREはいずれもメラノソーム上に局在する(画像4~6)。 2. メラノサイトにおいて内在性のSNAREタンパク質(シンタキシン3、SNAP23、VAMP7)は複合体を形成する。 3. シンタキシン3、SNAP23、VAMP7を特異的にノックダウンすることにより、メラニン合成酵素Tyrp1やチロシナーゼがメラノソーム上から消失する(画像7・8)。メラニン合成酵素の量が減少するため、結果的にSNAREノックダウン細胞においては細胞内のメラニン色素量が減少する(画像9)。 4. SNAREノックダウン細胞におけるTyrp1の消失は、メラノソームへ正しく輸送されなかった分子が「リソソーム」と呼ばれる場所で分解されることにより引き起こされる(画像10・11)。
以上の結果から、マウスの培養メラノサイトにおいてメラニン合成酵素をメラノソームに受け渡すためには、3種類のSNAREタンパク質が不可欠であることが明らかになったというわけだ。VAMP7はTyrp1を含む小胞上に、シンタキシン3とSNAP23はメラノソーム上に局在すること、またこれらのSNAREタンパク質はメラノサイトにおいて複合体を形成することから、形成したSANRE複合体がメラニン合成酵素を含む小胞とメラノソームの膜融合を促進し、メラニン合成酵素がメラノソームに受け渡されるものと考えられるという(画像13)。
さらに、SNAREタンパク質をノックダウンした細胞では、メラニン合成酵素がメラノソームに正しく輸送されず、リソソームで分解されるため、結果的に細胞内のメラニン色素量が減少するという事実も明らかになった。その点に関して研究チームは、「興味深いこと」としている。

|
|
画像12。SNAREタンパク質複合体によるメラニン合成酵素のメラノソームへの受け渡しモデル。膜融合に関わるSNAREタンパク質複合体の機能が損なわれると、メラニン合成酵素はメラノソームに受け渡されず、細胞内の分解場所であるリソソームで壊されてしまう(赤矢印) |
今回の成果により、小胞輸送によって運ばれて来たメラニン合成酵素を正しく目的のメラノソームに受け渡すことができないと、メラニン合成酵素はリソソームで分解され、結果的に細胞内メラニン色素量が減少することが解明された。現在の美白化粧品の主流は、「チロシナーゼの活性」を抑えるものだが、今回の研究成果により「メラニン合成酵素の分解(メラノソームへの輸送を抑える)」をコンセプトとした新たな美白化粧品開発への応用が期待されると、研究チームは述べている。