理化学研究所(理研)は11月8日、塩基配列を変えることなく遺伝子発現を抑制する「RNA干渉法」により、体細胞クローンマウスの出生率を10倍以上改善する技術を開発したことを発表した。開発は理研バイオリソースセンター遺伝工学基盤技術室の小倉淳郎室長(筑波大学大学院生命環境科学研究科教授、東京大学大学院医学系研究科教授兼任)らによるもので、成果は「米科学アカデミー紀要(Proceedings of the National Academy of Sciences of the United States of America:PNAS)」のオンライン版に11月7日の週に掲載される予定。
体細胞クローン技術は核移植技術の1つであり、同じ遺伝情報を持った「コピー動物」を無限に生産できることから、畜産分野を初め、実験棟物を利用する制約や医療分野など幅広い応用が期待されている。
しかし、1997年に世界初の生体由来体細胞クローン羊「ドリー」が誕生して15年以上が経過したが、体細胞クローン動物の生産効率は著しく低いままで、移植した胚の数%しか生まれてこないのが現状だ。
これまでに研究グループでは体細胞クローンの効率が低い理由を確かめるため、マウスをモデルとしてさまざまなクローン胚特有の異常を探してきた。特に2010年には、網羅的な遺伝子発現解析の結果から、体細胞クローンの着床前胚(卵管で受精して子宮へ移動して着床する前の受精卵のこと)では性染色体の1つであるX染色体上の遺伝子群の多くが発現低下を示していることを見出し、その原因がX染色体上の遺伝子の発現を抑制する「Xist」(エグジスト)遺伝子の過剰発現であることを突き止めている。
さらに、Xist遺伝子を欠失したノックアウトマウスを用いて、体細胞クローンの産子作出の効率を10倍近く改善することにも成功した。しかし、この方法は遺伝子の欠損という遺伝子改変を伴うため、マウス以外の動物では技術的・法律的な壁があり、より簡便で実用可能な方法の開発が望まれていたのである。
ある特定の遺伝子の機能を抑える手法の1つに、遺伝子の欠損や挿入といった遺伝子改変を伴わず、一時的な発現抑制を引き起こす手段として、RNA干渉法がある。RNA干渉法は、特定の配列を持つ2本鎖RNAの導入により、相補的なメッセンジャーRNAの分解を促進させるというものだ。
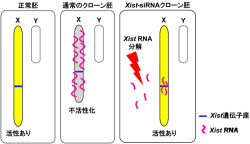
研究グループは、RNA干渉法を利用してXist遺伝子の過剰発現をできるという想定(画像1)のもと、Xist遺伝子の転写産物であるRNAに対して相補的な「short interfering RNA」(siRNA:RNA干渉を引き起こす21から23塩基配列の短いRNA鎖のこと)を設計し、これを各移植直後の状態である1細胞期の雄のクローン胚に注入した。
|
|
画像1。RNA干渉法による体細胞クローン胚でのXist発現抑制の模式図。体細胞クローン胚では、正常な雄胚では発現しないはずのXist遺伝子が過剰発現することで、X染色体上の遺伝子群の発現を抑制してしまう。一方、Xist遺伝子に対するsiRNAを注入したクローン胚では、RNA干渉効果によって、Xist遺伝子の過剰発現が抑制される |
X染色体が2本存在するメスでは、正常なX染色体とXist遺伝子が過剰発現するX染色体を識別することが難しいため、今回はX染色体を1本しか持たない雄のクローン胚を用いた形である。
結果、通常のクローン胚では着床前期を通してみられるXist遺伝子の過剰発現を、桑実胚(子宮着床前の受精卵の内、8細胞胚以降の分裂をした、胎盤胞よりは前の胚のこと)期までに限って一時的に抑制することに成功した(画像2)。

|
|
画像2。着床前の体細胞クローン胚におけるXist遺伝子の発現パターン。(A)Xist遺伝子の発現レベル。(B)Xist遺伝子の転写産物RNAの局在。通常のクローン胚ではXist遺伝子が過剰発現し核内に蓄積してくる(ピンク)が、siRNAを注入したクローン胚ではXist遺伝子の過剰発現が抑制され、桑実胚期までその効果が続く |
この時得られた桑実胚期クローン胚の遺伝子発現を網羅的に解析すると、X染色体上の遺伝子だけでなく、常染色体上の多くの遺伝子群もその発現が正常化していることが判明した。
次に、これらXist遺伝子の発現を抑制したクローン胚の発生能を評価するため、このクローン胚をマウスの卵管へ移植して、着床後の胚発生を解析。着床直後に当たる胎齢5.5日目で胚を観察したところ、siRNAを注入しない通常のクローン胚では多くの胚が発生異常を起こし、正常な形態の胚は1%程度しかなかった。
一方、siRNAを注入してXist遺伝子の発現を抑制したクローンでは、通常の10倍以上の効率(移植胚当たり16%)で正常な携帯の胚が得られたという次第である。この胚発生能の改善効果はその後も続き、出生児でも通常に比べて10倍以上の効率(移植胚当たり最高で20%)でクローン産子が生まれた(画像3)。

|
|
画像3。Xist遺伝子の発現抑制によって生まれたクローン産子。通常マウスの体細胞クローンは1腹から平均0.5匹程度の出産であるが、Xist遺伝子発現の抑制によって、1腹から最大で7匹のクローン産子が産まれた |
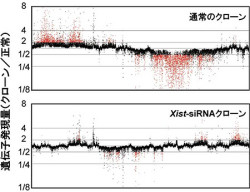
さらに興味深いことに、この産まれた産子の肝臓での遺伝子発現を網羅的に解析したところ、通常のクローン産子に見られる遺伝子発現の乱れが大幅に改善しており、着床前期の一時的なexist遺伝子発現抑制効果が出生後の遺伝子発現にまで影響していることが判明した(画像4)。
|
|
画像4。クローン産子における遺伝子発現パターン。出生直後の正常産子とクローン産子の肝臓における遺伝子発現パターンを比較すると、Xist遺伝子の発現抑制によって、異常を示す遺伝子数が大幅に減少する。赤い点は正常産子と比べて2倍以上の発現上昇もしくは発現抑制を示した遺伝子 |
今回のRNA干渉法は遺伝子改変を伴わず、卵子や胚に直接siRNAを注入するという非常に簡便な技術であり、幅広い動物胚にそのまま応用可能な技術であることが特徴だ。実際に、牛やブタなどの体細胞クローン胚でもXist遺伝子が過剰に発現することが知られていることから、RNA干渉法によるXist遺伝子の発現抑制はこれらの畜産動物を用いたクローン技術においても有用出る可能性があるとしている。