理化学研究所は9月19日、水素の挙動を観察できる新たな水素吸蔵材料「多金属ヒドリド(H-)クラスター」の合成と構造解析に成功したことを発表した。中国大連理工大、仏・ラウエ-ランジュバン研究所、米・南カリフォルニア大との共同研究で、今回の成果は科学雑誌「Nature Chemistry」オンライン版に日本時間9月19日に掲載された。
水素は燃焼しても水になるだけで、温室効果ガスを排出しないクリーンで再生可能なエネルギーとして注目されているのはご存じの通り。燃料電池の燃料としての実用化を目指してさまざまな研究や開発が行われているが、化石燃料と異なって常温・常圧だと機体のため、輸送や貯蔵の難しさが普及の妨げとなっている。
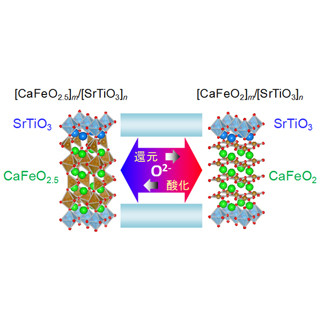
その解決策として期待されている方法の1つが、水素を「ヒドリド」(H-)の形で金属と結合させ固体にする貯蔵法だ。この方法のメリットは、用いる材料によらずに水素の体積を1/1000以下に抑えることができ、かつ使用したい時には水素として取り出せる点である(画像1)。
しかし、世界規模で新しい水素吸蔵材料の開発が競うようにして進められているが、実用化するにはまだ多くの課題が残っているのが現状だ。固体中での詳細な調査が困難なためで、中でも水素を吸着した後の構造やその反応プロセスの詳細がわかっていない。
分子の立体構造を調べる手段としてX線構造解析があるが、この方法は電子密度の分布を明らかにする方法のため、多くの電子を持つ金属原子近傍に位置し、電子を1つしか持たない小さな水素の発見は難しいという点がある。
その一方で、水素を含む金属-ヒドリド化合物の構造が明らかになった化合物もあるのだが、それらの多くは水素の出し入れが自由にできないという欠点があるという具合だ。
そうした中で、研究グループはこれまでに希土類-ヒドリドの結合を持つ希土類ヒドリド化合物の性質や反応を明らかにした実績を持つ。希土類金属は、電子的にプラスになりやすいため、それと結合を持つヒドリド原子はマイナスになりやすいという特性がある。そのため、X線構造解析でも比較的容易に水素の位置を決められるというわけだ。
だが、そんな希土類金属だけでは、肝心の水素の吸着や放出を行えないという大きな欠点がある。そこで研究グループは、希土類ヒドリド化合物を基にd-ブロック遷移金属を組み合わせ、分子構造が明確でしかも可逆的に水素を吸着・放出することが可能な異種金属混合型の多金属ヒドリドクラスター(異種多金属ヒドリドクラスター)の実現を予測し、その合成と水素との反応プロセス解明に挑んだというわけである。
研究グループは、まず2003年に開発した希土類ヒドリド化合物と、モリブデンやタングステンのヒドリド化合物を組み合わせることで、異種多金属ヒドリドクラスターの合成に初めて成功(画像2・左)。
そして、その分子構造をX線および中性子線で解析した結果(画像2・右)、両者の結果はほぼ等しく、金属を結ぶすべてのヒドリド原子の精密な位置が確認できたという次第だ。

|
|
画像2。異種金属混合型の多金属ヒドリドクラスターの構造。左は、合成した異種金属混合型の多金属ヒドリドクラスターの全体構造。Mはモリブデンやタングステン、Hはヒドリド、Yはイットリウム。SiMe3、Me3Siはトリメチルシリル基。右は中性子回折で得られたコア構造。赤(電子的にプラス)と青(電子的にマイナス)で囲ったヒドリド原子は、互いに異なる電荷を持ち、混ざり合わないという特徴を持つ |
また、モリブデンやタングステンだけと結合するヒドリド原子はプラスの電荷を帯び、イットリウムだけとの結合だとマイナスの電荷を帯びることも判明。お互いに電子的な性質が異なり、混ざり合わないことも確認されている(図2・右)
この異種多金属ヒドリドクラスターを減圧下で「加熱脱気」(10-8乗気圧、80℃)とすると、水素1分子を放出した新たなクラスターが得られたとした(画像3・右)。その構造を調べたところ、中心部にあったヒドリド原子と、2つのイットリウム原子間(Y3とY4)を架橋していたヒドリド原子が、水素分子となって放出していることが判明している(画像3・左→右)。
そして、この水素分子が抜けた抜けた多金属ヒドリドクラスターに再び水素を常温・常圧で吹きかけると、速やかに水素を吸着し、元のクラスターに戻ることが確認された(画像3・右→左)。

|
|
画像3。可逆的な水素付加・脱離反応と電車のパンタグラフ。減圧下で加熱脱気すると、赤丸で示したヒドリド原子が水素分子として抜けていく。金属フレームは電車のパンタグラフをたたむように空いたスペースを埋めている |
さらに、水素がこの単結晶に吸着する様子をX線構造解析で追跡したところ、水素と反応してヒドリド原子が中心部とY3~Y4の間に取り込まれる様子と全体構造の変化を、リアルタイムでとらえることに成功している(画像4)。理論計算による解析の結果、この水素との反応では、イットリウムが水素を捕らえ、モリブデンが水素を蓄えることでクラスター内に水素が取り込まれることが判明した。

|
|
画像4。結晶状態を保持したまま水素と反応する様子。上は、水素との反応の式。中は、結晶の写真。結晶が水素と反応し構造が変化するため、結晶自体の色が黒から赤に変化していく。下は、差電子密度図。電子密度の変化(紺色)とその位置により、ヒドリド原子が徐々に増えていく様子が確認できる |
研究グループでは、今回の成果は、より多くの水素を効率よく吸着・放出するための「金属の組み合わせ」や「金属の電子的性質が反応性に夜ボス影響」についての理解を深め、今後さらに新たな物質群の創製や、それらの研究を通した新たな水素吸蔵材料への開発につながると期待するとしている。また、これまで1つの金属に集中した研究がほとんどだったが、多数の金属が反応に作用する多金属クラスターを用いた新たな触媒の開発などへの展開も期待されているとした。