北海道大学(北大)と産業技術総合研究所(産総研)は4月25日、ミトコンドリアの機能に関与する硫黄修飾酵素が、酸素に接すると崩壊する不安定な鉄硫黄クラスターを用いて機能することを同定したと発表した。
同成果は、北大大学院先端生命科学研究院 田中良和准教授(研究当時、現東北大学大学院生命科学研究科教授)、産総研創薬基盤研究部門 鴫直樹主任研究員らの研究グループによるもので、4月24日付の米国科学誌「Proceedings of the National Academy of Sciences of the United States of America」に掲載された。
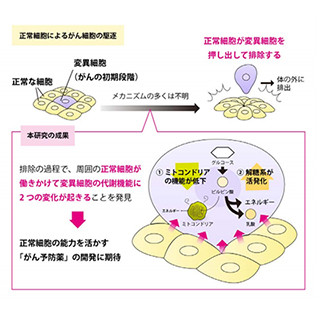
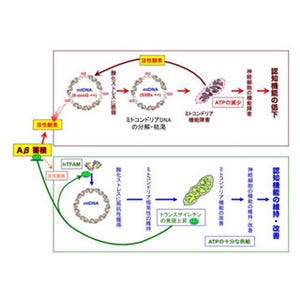
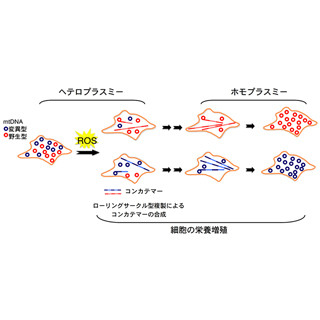
細胞のエネルギーを生産する細胞小器官であるミトコンドリアの活動は、転移RNAの硫黄修飾と関連が深いことが近年報告されており、ミトコンドリアの機能を制御する新たな経路が予想されていた。硫黄修飾の一種である2-チオウリジン修飾は、真核生物において、ミトコンドリアの機能に深く関与していることが知られているが、その制御機構の詳細については不明な点が多く残されている。
同研究グループは今回、好熱性真正細菌由来2-チオウリジン合成酵素「TtuA」の構造機能解析を実施。この酵素が、酸素に接すると崩壊する不安定な「鉄硫黄クラスター」という因子を用いて硫黄を転移することを突き止めた。これまで細胞質中の2-チオウリジン生合成機構が明らかにされてこなかったのは、従来の実験が大気環境下で行われていたことから、この鉄硫黄クラスターが崩壊していたためであったと考えられるという。
また同研究グループは、複合体構造解析の結果から、TtuAが鉄硫黄クラスターをあたかもタンパク質の一部のように用いて硫黄を転移するという、これまで知られていない硫黄修飾メカニズムを用いることを提唱した。
同研究グループは今回の成果について、ミトコンドリアによるエネルギー生産の制御機構を解明するための重要な手がかりを与えるものと説明している。