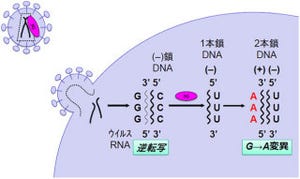
日本原子力研究開発機構(JAEA)は、大型放射光施設(SPring-8)のX線を用いて、生体内のDNAが放射線によって損傷を受ける際に、これまでに知られていない損傷機構があることを発見したと発表した。
同成果は、同 先端基礎研究センター放射場生体分子科学研究グループの岡壽崇博士研究員(現 大阪大学産業科学研究所 特任助教)と同 横谷明徳グループリーダー、東京農工大学大学院工学研究院の鵜飼正敏 教授らの研究チームによるもので、詳細は米国物理学会誌「Physical Review Letters」電子版に掲載された。
放射線の中でもイオンビームなどの高速の荷電粒子が撃ち込まれた細胞中では、荷電粒子がさまざまな大きさのエネルギーをDNA分子に与え、そのエネルギーに応じ、多様な損傷プロセスが同時並行的に進行する。しかし、従来そうした個々のプロセスを抽出、解析する手法がなかったことから、DNA損傷プロセスの全貌は明らかになっていなかった。
これまでDNA分子に特定エネルギーのX線を選択して照射する方法としては、シンクロトロン放射(放射光)が用いられてきた。1keV以下のX線領域には、DNAを構成する酸素や窒素の内殻電子をイオン化する帯域(K殻吸収端)が含まれており、放射光を分光器と呼ばれるエネルギー選別装置を通して、そのイオン化レベルを超えるエネルギーのX線を取り出し照射することで、DNA分子中に、特定のイオン化現象を起点とするDNAの損傷過程を調べることが可能と考えられきた。
DNA損傷に至る過程では、最外殻の電子軌道に1つだけ存在している電子で反応性に富む不対電子を有する反応中間体を経由すると考えられている。しかし、これは不対電子を含む部位の寿命を短くしている原因でもあり、不対電子の直接観測は困難であった。これまでは照射後のDNA試料を極低温に保持しながら電子常磁性共鳴(EPR)装置まで運搬して不対電子を測定するため、搬送中に消失してしまう不安定な不対電子は測定できないなど多くの問題があった。
研究チームは今回、SPring-8の放射光の特性を生かし、特定のエネルギーに選別した後でも十分な強度を持つ細いX線ビームを直接EPR装置内に導入し、DNA薄膜試料への照射を行った。このEPR装置はDNA放射線損傷の研究のためにSPring-8のビームライン(BL23SU)に常設された設備で、これを用いることで、運搬による不対電子消失の問題を解決し、DNA分子中に生じた不安定な不対電子の生成量を、EPR信号強度として「その場」観察することが可能となった。
照射するX線のエネルギーを少しずつ変えることで、DNA分子を構成する窒素および酸素原子のK殻電子のイオン化レベル付近において不対電子の生成量がどのように変化するかを詳細に調べた結果、K殻電子がX線を吸収する確率に対応して不対電子の生成量も変化することが判明したほか、イオン化レベルをわずかに超えたエネルギーのX線を照射した場合、DNAのX線吸収確率に基づいた予想を超え異常にEPR信号が増大することが明らかになった。
|
|
|
窒素および酸素のK殻吸収端におけるEPR信号の異常な増大。EPR信号強度の照射X線エネルギー(横軸)に対する変化(左軸:赤線)をDNAによるX線吸収確率のそれ(右軸:青線)と比べると、窒素および酸素のK殻吸収端をわずかに超えた領域(○で示された部分)でEPR信号強度が異常に増大していることが判明した |
物質がX線を吸収する場合、イオン化レベルをわずかに超えたエネルギーでは、原子から離脱しようとする一対の電子のうちの1つが、その途中で再び原子に捕獲される現象「衝突後相互作用(Post Collision Interaction:PCI)」が生じる。こうした再捕獲がある場合、高いエネルギーの軌道に電子が1つだけ残されるため、これがEPR信号強度の増大原因であることが予測されるため、このようなPCIを考慮した理論計算を行った結果、実験データをうまく説明できることが判明したという。
近年の研究では、放射線照射によってDNA薄膜から放出された2次電子が試料中で減速された後にDNA分子の別の部位に付着して、DNA分子鎖を結合解離させて損傷生成に至ると報告されていたが、今回の生体分子にPCIの効果を見出された例は初めてで、このような解離性電子付着現象とは異なる、特定のエネルギーで生じるイオン化プロセスに関係したDNA損傷の生成過程が存在することが示されたものとなったという。
なお研究チームでは、今回の結果は、高速荷電粒子線を含む放射線が生体に与える影響の原因となるDNA損傷の生成過程に関する重要な基礎的知見となり、これにより放射線の中でも特にガンの放射線治療や植物の育種に用いられる高速荷電粒子線が生体中でどのようにDNA分子を変化させていくか、その初期過程の解明を目指した研究を進展させることになるものとの期待を示している。