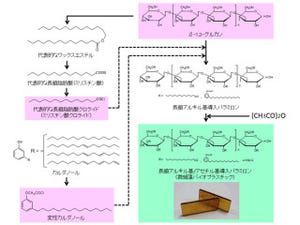
筑波大学などの研究グループは、アルドキシム化合物を脱水反応によってニトリル化合物に変換する「アルドキシム脱水酵素(OxdA)」の分子構造をX線結晶構造解析法により決定。酵素反応中心のヘム鉄および周辺のアミノ酸残基の役割を解明し、炭素-窒素三重結合形成の反応メカニズムを明らかにしたと発表した。
同成果は同大 大学院生命環境科学研究科の小林達彦 教授、同 野村純平 大学院生、同 橋本義輝 助教、同 和田浩一 大学院生、同 老沼研一 助教、横浜市立大学大学院生命ナノシステム科学研究科の橋本博 准教授、九州大学先導物質化学研究所の成田吉徳 主幹教授、同 太田雄大 助教らによるもの。成果の詳細は、米国科学アカデミー紀要「Proceedings of the National Academy of Sciences of the United States of America(PNAS)」オンライン速報版にて公開された。
C-N三重結合のシアノ基を有する高い毒性を有する化合物の総称である「ニトリル」は現在、化学工業の出発物質あるいは合成中間体として用いられている。しかし、そうした工業分野では高温かつ強酸性といった条件のもと用いられており、より安全かつ高効率な合成が可能な触媒もしくは生体触媒を用いて生化学反応を行うバイオリアクターとして機能する酵素の発見が求められてきた。
小林教授の研究グループはこれまでの研究から、細菌に属するニトリル分解菌である「Pseudomonas chlororaphis B23」株において、酵素ニトリルヒドラターゼによるニトリル分解系と、活性中心にヘム鉄を含み、有機基質(アルドキシム)が直接、ヘム鉄に結合することで化学反応が進行する酵素「OxdA」によるニトリル合成系が遺伝子および代謝上、リンクしていることを発見してきているが、今回の研究では、Pseudomonas chlororaphis B23菌から単離したOxdA遺伝子を大腸菌の体内に組み込み、その組み換え大腸菌にOxdAを発現させた後、高純度まで単離精製することに成功したという。
また、橋本淳教授の研究グループが、その酵素を用いてOxdAを結晶化し、その結晶を用いてつくばフォトンファクトリーの放射光X線を用いた解析を実施したところ、OxdA酵素の立体構造を1.8Åの分解能が決定されたという。さらに、研究グループでは部位特異的変異法や分光学的手法などを用いた実験を実施したところ、活性中心近傍の種々のアミノ酸を人為的に変異させた酵素の発現に成功し、各変異酵素の活性をはじめ酵素化学的諸性質の解明を果たしたほか、成田教授および太田助教の研究グループでは、化学的環境に感度良く応答する一酸化炭素を各種OxdAのヘム鉄に結合させ、その振動構造を共鳴ラマン分光法を用いて解析し、酵素の活性中心を構成するアミノ酸の役割の解明を行ったという。
これらの実験を行った結果、セリン219が基質とヘム鉄の結合の安定化に貢献していること、ならびにヒスチジン320が酸塩基触媒として働くこと、そしてアルギニン178の側鎖がヒスチジン320のイミダゾール環の求電子性を増加させていることが明らかになった。これを受けて研究グループでは、ニトリル合成の酵素反応メカニズムの全貌が解明されたと説明しており、将来的にはバイオテクノロジーにより低い環境負荷でニトリル化合物を工業的に合成するための技術につながることが期待されるとしている。