東北大学大学院医学系研究科、東北大医学系グローバルCOE、東京大学先端科学技術研究センター、国立がん研究センターは7月10日、がん細胞の悪性化をもたらす代謝制御メカニズムとして、正常細胞中で酸化ストレス応答を担う転写因子(制御タンパク質)の「Nrf2」が、がん細胞の中では糖やアミノ酸の代謝を変化させることにより、がん細胞の増殖を促進することを突き止めたと共同で発表した。
成果は、東北大大学院 医学系研究科 ラジオアイソトープセンターの本橋ほづみ准教授、同医化学分野の光石陽一郎博士、洞田口恵子助教、洞山本雅之教授、東大先端科学技術研究センターの油谷浩幸教授、がん研 がんゲノミクス研究分野の柴田龍弘分野長らの研究グループによるもの。研究の詳細な内容は、米学術誌「Cancer Cell」7月10日号に掲載された。
がん細胞は活発に増殖するために、細胞構造の材料となるタンパク質、脂質、核酸を大量に合成している。この代謝制御の仕組みを解明することは、抗がん治療に直結すると期待され、注目を集めている状況だ。
1980年代以降、がんは日本人の死因の第1位である。とりわけ、肺がんによる死亡率はがんの中でも特に高く、男性では第1位、女性では大腸がんに次いで第2位だ。また、手術療法、化学療法、放射線療法などの治療法の進歩にもかかわらず、肺がんの生存率は5年と、ほかのがんと比較して低迷している。
そして国がん研並びに東北大は、世界に先駆けて、Nrf2が「非小細胞性肺がん」で高頻度に活性化型変異を起こしていることを発見した実績を持つ。Nrf2とは、本来、酸化ストレス応答や異物代謝などの生体防御機構で中心的な役割を果たしている転写因子だ。
このNrf2が強く発現している肺がん症例では、予後が極めて不良であることが、両機関を含めた複数の施設から報告され、肺がんの悪性化を担っているタンパク質の1つがNrf2であることを明らかにした。さらに、肺がん以外でも食道がんや胆嚢がんなどで、Nrf2が異常に安定化して核内に蓄積している症例が多数発見されている。
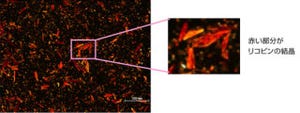
通常の状態では、Nrf2タンパク質は細胞質で常に分解されており、その存在はほとんど検出できない。一方、細胞が酸化ストレスや毒物などに曝露されると、安定化して核内に蓄積し、DNAに結合して生体防御に重要な遺伝子群を活性化する。その結果、抗酸化タンパク質や解毒酵素が誘導されて、細胞の障害は最小限にとどめられる仕組みだ(画像1)。
Nrf2は、これまでがん細胞の悪性化に働くメカニズムとして理解されてきた。がん細胞でNrf2が恒常的に安定化すると、生体防御遺伝子群が常に活性化され、その結果、がん細胞は抗がん剤や放射線照射に対する抵抗性を獲得すると考えられてきたのである。
しかし、Nrf2が高いレベルで発現しているがん細胞では、細胞の増殖そのものが亢進していることも観察されており、このこともNrf2のがん細胞での働きと理解されてきたが、これまではそのメカニズムそのものは解明されていなかった。
そして今回の研究で、Nrf2が、肺がん細胞において活性化する遺伝子を網羅的に調べたところ、「グルコース」と「グルタミン」の代謝に関与する酵素群の遺伝子が直接Nrf2により活性化されることが判明。グルコースの代謝経路の内、「ペントースリン酸経路」を触媒する主要な4酵素がNrf2の標的遺伝子となっていることがわかった。
また、グルタミンの代謝経路の内、これまで知られていた「グルタチオン」の合成に関わる酵素に加えて、グルタミンから乳酸を生成する経路の酵素もNrf2により直接制御されていることがわかったのである。
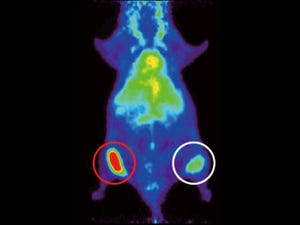
肺がん細胞において、Nrf2が代謝の流れにどのような影響を与えているかを調べると、Nrf2は核酸合成とグルタチオン合成を強力に促進することがわかった。これらはいずれも細胞の増殖にとって有利な同化反応だ。すなわち、Nrf2はグルコースを核酸合成へ、グルタミンをグルタチオン合成へと向かわせることで、細胞増殖に有利な代謝を実現していることが判明したのだ(画像2)。
画像2は、がん細胞においてNrf2がもたらす代謝への影響を表したものだ。増殖していない細胞において、Nrf2は主としてストレス応答を担っているが、がん細胞を含む増殖中の細胞では、グルコースやグルタミンの代謝に大きく影響を及ぼし、同化反応を促進するのである。
こうしたNrf2の代謝への影響は、増殖が盛んな細胞において特に強く認められることがわかった。増殖していない細胞では、Nrf2は主として酸化ストレス応答、解毒代謝機能を担っているが、増殖を促進する刺激が細胞に作用するとNrf2の機能が強まり、その結果、Nrf2はグルコースやグルタミンの代謝の流れを改変する作用を発揮できるようになることも判明したのである。
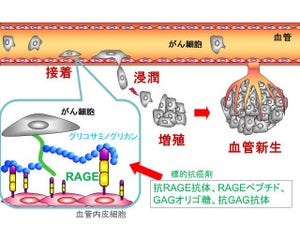
さらに、Nrf2機能の亢進は逆に増殖シグナルの増幅をもたらし、Nrf2機能と増殖シグナルとの間の正のフィードバック機構が細胞増殖をさらに促進していると考えられた(画像3)。
20世紀初頭にオットー・ワールブルグは、がん細胞が正常の細胞とは異なる特徴的な代謝様式を用いていることを発見し、その代謝様式は彼にちなんで「ワールブルグ効果」と呼ばれている。
最近ではこれに加えて、がん遺伝子の活性化、もしくはがん抑制遺伝子の欠落がもたらす特異な代謝経路が次々と報告されており、抗がん剤の標的として代謝酵素が注目されている状況だ。
ペントースリン酸経路は、核酸の合成に必須の代謝経路であるにも関わらず、これまではがん細胞におけるその促進機構は不明だった。今回の研究成果は、その直接の活性化因子がNrf2であることを明らかにしたものである。
また、酸化ストレス応答を担うはずのNrf2が、細胞の増殖刺激存在下において、代謝経路の改変をもたらして増殖を促進するという、がん細胞の悪性化メカニズムの新しい局面が明らかになった。
さらに、Nrf2の機能亢進と増殖シグナルとの間に存在する正のフィードバックの発見は、Nrf2を高発現するがんに対する、より効果的な治療戦略の開発に道を拓くものであると、研究グループは語っている。