大阪大学(阪大)は2月13日、標的分子「補体第5成分(C5)」の「遺伝子多型」(DNA配列の個人差)により、抗体医薬「ソリリス」に不応性を示す機序を解明したと発表した。
成果は、阪大大学院 医学系研究科 内科学講座 血液・腫瘍内科学教室の西村純一助教らの研究チームによるもの。研究の詳細な内容は、米国東部時間2月13日付けで「The New England Journal of Medicine」に掲載された。
「発作性夜間ヘモグロビン尿症(PNH:paroxysmal nocturnal hemoglobinuria)」は、血球膜上の「補体制御因子」を欠くため、補体活性化に伴い血管内溶血をきたす。PNHに対する溶血治療薬として、C5に対するソリリスが開発され、これまで欧米を中心に顕著な抑制効果が示されて来た。
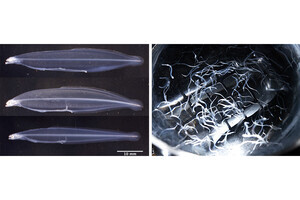
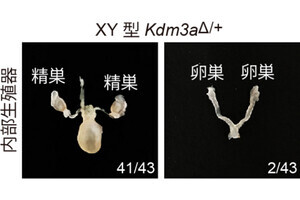
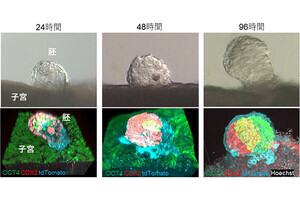
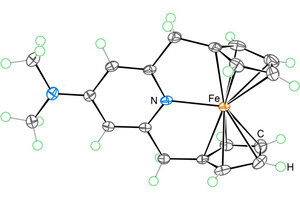
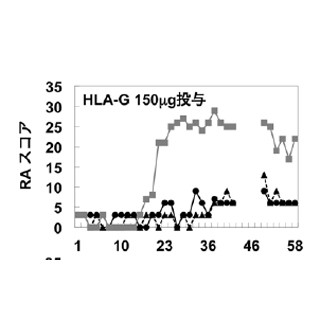
日本国内では2010年に承認となり、300例を超す症例に投与されているが、溶血がまったく抑制されない不応例も報告されている(画像1)。そこで不応例11例のC5遺伝子の解析がなされ、全例に共通のヘテロ変異「c.2654G>A」が同定された(画像2・3)。さらに、288例の健常人での解析も行われ、その内の10例において同変異が同定されたのである(保有率3.5%)。
なおヘテロ変異とは、変異した遺伝子と普通(野生型)の遺伝子の両方を持つ場合で、「ホモ変異」は変異した遺伝子を2つ持つ場合を指す。つまり、両親からもらった遺伝子の内、片親からだけのものが変異している場合がヘテロ変異、両親からもらった遺伝子の両方がそろって変異している場合はホモ変異というわけだ。
さらに同変異は、中国人(漢民族)120例中1例に同定されていたが、100例の英国人ならびに90例のメキシコ原住民には見出されなかった。この変異C5タンパク「p.Arg885His」を作成して機能解析が行われた結果、本来の機能である溶血活性は正常に保持されていたが、その抗体であるソリリスはまったく結合できないことが判明した。つまり、アジア固有のC5遺伝子多型により、その抗体医薬ソリリスに不応性をきたしている機序が明らかになったのである。
なお遺伝子多型とは簡潔にいうとDNA配列の個人差だが、集団の1%以上の頻度であるものと定義されることが多い。同じDNA配列の個人差でも変異(ミューテーション)とは異なり、それだけで大きな表現型の変化や、病気を起こさないものを指す。
ソリリスは欧米を中心に、PNHと「非典型溶血性尿毒症症候群(aHUS)」において承認され、顕著な有効性が示されている。さらに、「視神経脊髄炎」や重症筋無力症など補体関連疾患において適応拡大が期待されているという。また、アジアにおいては日本を中心に投与されているが、今後韓国、中国など急速に普及していくことが予想され、不応性の原因となるアジア固有の遺伝子多型を同定したことは意義深いこととした。
現在、多くの抗体医薬が分子標的治療の主力として世界中で繁用されているが、ソリリスは極めて効果が顕著な薬剤で、さらに今回のようにまったく効果が見られない不応例の報告も、「耐性突然変異」(薬剤に耐性を示すような変異を後天性に獲得すること)の出現例以外の報告はない。このような状況下で、不応性の機序として遺伝子多型が証明されたことは、今後、抗体医薬の反応性を検証する上で大変意義深いとしている。