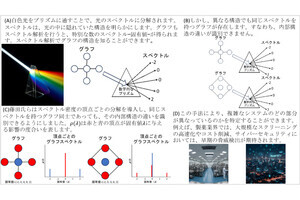
東京工業大学(東工大)は1月22日、薬剤や生体適合性材料として重要な「ペプチド」を迅速、高収率、かつ安価に合成する手法を開発し、同手法により安価で高活性な試薬を使用して「マイクロフロー合成法」を駆使することで反応時間を5秒以内に制御し、副反応の抑制に成功したと発表した。
成果は、東工大大学院 理工学研究科の布施新一郎助教、同・大学院生の御舩悠人氏らの研究チームによるもの。研究の詳細な内容は、2013年12月3日付けで独化学会誌「Angewandte Chemie International Edition」に掲載され、「Synlett」にも掲載予定だ。
ペプチドはアミノ酸が「アミド結合」で連結した化合物であり、長いペプチドが折り畳まれたものがヒトの体を構成するタンパク質というわけだ。現在のペプチドの化学合成は、アミド結合形成に伴う最も問題となる副反応である「エピメリ化」を抑制するため、「カルボン酸[-(C=O)OH]」を高価な試薬により穏やかに活性化し、数時間以上をかけて目的物を得るのが一般的となっている(エピメリ化は、カルボン酸を活性化した際にα位の立体化学が反転した化合物が生じてしまう反応)。この際、基質によって適切な試薬が異なるため、事前の試薬のスクリーニングが必要なことがあり、労力・時間を要していた。
また、試薬に由来する多量の副生物が目的物と共に得られるため、目的物の精製が困難となることも珍しくない。さらには、高価な試薬を用いても嵩高いアミノ酸や非常にエピメリ化しやすいアミノ酸を用いた際には、十分な収率で目的物が得られないことがあり問題となっていた。
つまり、(1)高価な試薬を要する(2)試薬のスクリーニングが必要(3)多量の副生物を生じる(4)嵩高いアミノ酸との反応は長時間かかる、という問題点があったのである。このため多様なアミノ酸から構成されるペプチドの大量・低コスト供給は極めて困難だった。これらの問題により、米国化学会からも2007年にはアミド結合形成反応は工業的観点からも最も改善すべき反応の1つとされている。
研究チームは今回の実験に際して、「マイクロフロー合成法」を駆使した効率的な有機合成手法の開発に取り組んできたそれまでの経験を、従来の合成法の問題解決に生かせないかと考察。つまり、これまでのペプチド合成で常識とされてきた「長時間の穏やかな活性化」ではなく、マイクロフロー合成装置中での「短時間の迅速な活性化」という新しい概念に基づくペプチド合成を着想したというわけだ。
マイクロフロー合成法とは、微小な流路を反応場とするマイクロフロー合成装置を駆使する手法のことをいう。旧来のフラスコなどを用いる「バッチ合成法」と比較して、反応時間(1秒未満も可)、反応温度の厳密な制御が可能なのが大きな特徴だ。
そこで研究チームは実際にマイクロフロー合成法を駆使し、安価・高活性・低毒性の試薬である「トリホスゲン」(毒性の高いホスゲン三分子からなる化合物)を用いて、0.5秒、20℃でカルボン酸を活性化し、4.3秒でアミド化することにより、合計でもわずか4.8秒で、副反応を抑制しつつアミン(-NH2)と反応させて高収率で目的ペプチドを得ることに成功した。このように秒単位での反応時間の厳密な制御、精密な温度制御により、エピメリ化などの副反応の抑制が可能となったというわけだ。
マイクロフロー合成法は連続・並列運転によりスケールアップが容易で、副生物が少なく、エピメリ化を起こしやすいアミノ酸(例:フェニルグリシン)や、嵩(かさ)高いアミノ酸にも適用可能であり、おおむね収率9割以上、エピメリ化3%以下で目的物を得られる。また、有毒なホスゲンは装置内で発生・消費されるため、一切装置外には排出されない仕組みだ。
なお嵩高いアミノ酸とは、ここでは窒素原子上にメチル基を持つ「N-メチルアミノ酸」や五員環の中に窒素原子が存在する「プロリン」などを指す。これらのアミノ酸は反応する窒素周辺に置換基を持つため、これが反応の際の障害となり、一般的に反応性が低いのである。
マイクロフロー合成法は前述したように容易にスケールアップが可能なことから、工業法への展開も十分期待できるという。現在、開発された手法の有用性を実証するため、生理活性ペプチドの合成が推進されており、さらにその先には多段階アミド結合形成反応を連続的に行う手法の開発も見据えられている。これにより、将来は多様なアミノ酸から構成される有用ペプチドの大量・低コスト供給につながると期待しているとした。