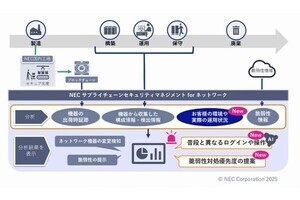
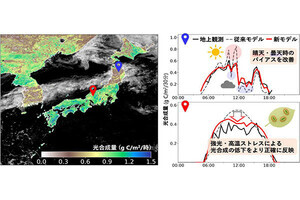
医薬基盤研究所(NIBIO)は、ヒトiPS細胞由来肝幹前駆細胞(肝細胞への分化の前段階の細胞)を安定に維持・増幅する技術開発に成功したと発表した。
同成果は、大阪大学大学院薬学研究科の水口裕之教授(医薬基盤研究所招聘プロジェクトリーダー併任)らによるもの。詳細は米国の幹細胞関連雑誌「Stem Cell Reports」に掲載された。
肝細胞移植は肝臓の移植に比べ侵襲性が少なく、安全性の面で優れていると考えられているが、1人の患者であっても大量の細胞を必要とするため、ドナーの絶対的不足が問題となっている。また、ヒト初代培養(凍結)肝細胞は、均一な品質を安定的に供給することが難しいという問題もあり、ヒトiPS細胞の活用によるそうした問題の解決に期待が高まっている。
これまで研究グループでも、ヒト肝細胞と同等の薬物代謝酵素の遺伝子発現量を有するヒトiPS細胞由来分化誘導肝細胞を作製していたが、実際に肝細胞移植などの再生医療や創薬への応用を行うには、分化誘導肝細胞を大量に準備する必要があるにも関わらず、分化には3週間以上かかることや、分化誘導した成熟肝細胞の増殖能が低いため、大量の成熟肝細胞を調整することが難しかった。
一方、成熟肝細胞の前駆体「肝幹前駆細胞」は高い増殖能を持ち、短期間で肝細胞へと分化できるため、肝幹前駆細胞を増殖する技術が開発されれば、肝幹前駆細胞から肝細胞への分化誘導技術と組み合わせることにより、大量の肝細胞の供給が可能になると考えられているが、ヒトiPS細胞由来肝幹前駆細胞を肝幹前駆細胞としての性質を保持させたまま、維持・増幅させる技術はこれまで開発されていなかった。

|
|
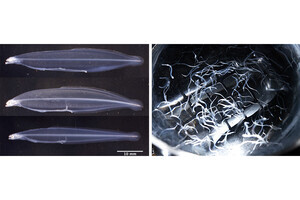
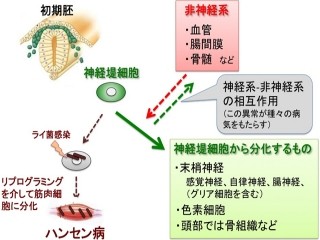
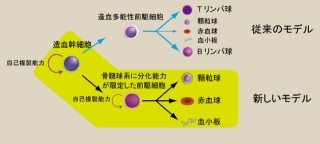
ヒトiPS細胞から肝細胞への分化誘導と肝幹前駆細胞の増幅。ヒトiPS細胞は、内胚葉、肝幹前駆細胞を経由して肝細胞に分化する。研究グループの今回の研究から、肝幹前駆細胞の増幅が実現され、それにより大量の肝細胞の供給を可能となった |
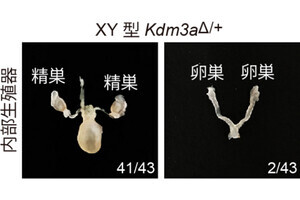
そこで今回研究グループは、ヒトiPS細胞由来肝幹前駆細胞を、細胞外マトリックスの構成部分であるラミニン111上で培養することで、細胞数にして最高1010倍の増幅を、肝幹前駆細胞としての性質を保持したまま実現する技術を開発。増幅した肝幹前駆細胞が成熟肝細胞のマーカーを発現する細胞や、もう一方の分化能である胆管細胞のマーカーを発現する細胞に誘導できることを確認したとするほか、継代を重ねた肝幹前駆細胞を、肝障害を起こした免疫不全マウスに移植したところ、マウス血中にヒトアルブミンを確認、invivoにおいても機能することを確認したとする。
なお、今回開発された同技術は、肝幹前駆細胞から肝細胞への分化を1ステップで行うことが可能なことから、ヒトiPS細胞由来分化誘導肝細胞の今後の実用化、コスト削減の意味で重要になると研究グループでは説明しており、今後は、増幅した肝幹前駆細胞から分化した肝細胞を用いて薬物の毒性評価系への応用を進めるとともに、肝幹前駆細胞の増幅条件を細胞医療に適した方法(血清や異種動物成分を含まない条件)に改良を行っていくことで、肝細胞移植や再生医療への応用への基盤技術の確立を図っていきたいとしている。