産業技術総合研究所(産総研)は5月7日、タンパク質などを対象として単結晶を1個だけ得るための技術を開発したと発表した。成果は、産総研生産計測技術研究センター 生化学分析ソリューションチームの宮崎真佐也研究チーム長、山下健一主任研究員らの研究グループによるもの。研究の詳細な内容は、3月21日付けで科学誌「Chemical Communications」オンライン版に掲載された。
結晶構造解析によりタンパク質の立体構造を知ることは、構造生物学における最も有効な手段の1つだ。生命現象の分子レベルでの理解や、医薬品開発に代表される産業応用に至るまで、幅広い分野の基盤的知見である。
近年、放射光の利用や機器の発達により、小さな結晶であっても結晶構造解析を行えるようになってきた。一方で、複数の単結晶が合体したり、密集したりするなど、結晶が重なり合うと解析が行えないという問題点は解決できていない。つまり、大きな単結晶を作成することよりも、1個だけ、または離ればなれの単結晶を得ることのほうが、より重要になってきているというわけだ。
これまで、宇宙環境を利用した単結晶作成の研究が行われてきている。微小重力下では、液体の「密度差対流」(重力のある環境では、重いもの(密度が大きい)ものが下に、軽いもの(密度が小さい)が上に移動しようとし、そのような移動が生じる際の流れのことをいう)が起こらないため、液滴内部では「マランゴニ対流」(表面張力が場所によって違う場合に発生する流れのことで、温度が均一であれば界面で生じる)だけが起こる。
そのような、特殊な物質の移動環境では、「拡散律速」によるタンパク質の結晶成長が可能となるため、一般的に、宇宙で得られる単結晶は大きくて結晶格子の完全性が高い。なお拡散律速とは、分子や原子などの物質の移動が、現象の全体の速さを決めている状態のことをいう。今回の研究では、タンパク質の移動速度が、結晶の成長速度を支配している状態のことを示している。
このように宇宙という環境は結晶成長にとってとても好都合ではあるが、簡単に行けないという大きな問題もある。現在は国際宇宙ステーションなどを利用することは可能だが、確実に利用できるという保証はないし、実験できたとしても当然ながら時間も限られるのはいうまでもない。よって、シミュレーションや地上での微小重力代替環境のような、低コストで扱いやすい結晶成長法が望まれているというわけだ。
産総研は、これまでにマイクロ流体技術を利用したさまざまな研究開発を行ってきており、その中の1つとして、微小液滴に関する研究を行っている。マイクロ流体技術は、狙った大きさの液滴を均一性を高く、大量に作成できるというものだ。
微小液滴は、特徴的な内部流体挙動を示すことが知られている。すなわち、強い表面張力により内部の流動は、密度差によって駆動される対流ではなく、マランゴニ対流が支配的となるのだ。
今回、地上での微小液滴の内部流体挙動が、微小重力下の液滴(必ずしも「微小」ではない)の内部流体挙動に類似していることが着目され、微小液滴を用いて、結晶成長に関する研究が行われた次第である。同時に、内部に1個だけ結晶を成長させるための液滴の大きさの計算法についても研究が行われた形だ。
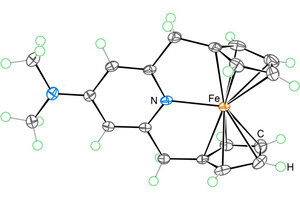
今回、微小液滴の調製には、画像1に示した「マイクロリアクター」が用いられた。マイクロリアクターとは、1mm以下程度の太さの細い流路に液体を送液しながら化学反応を行う反応器の総称のことだ。その流れが層流であり、温度制御性や化学反応の制御性に優れる。また、さまざまな形状の流路、バルブのような機械的構造や分析検出機構との統合により、必要な部材を1つの基板の上にまとめ、「Lab-on-a-chip(チップの上の実験室)」と称されることもある。
今回のマイクロリアクターは、3種類の溶液(タンパク質溶液、沈殿剤溶液、フッ化物オイル)を合流させて微小液滴とするチップ部分と、その微小液滴を貯蔵する「キャピラリー」(マイクロリアクターを構成する構造の内、細長い円筒管の部分のこと)部分から構成されている。
このようなマイクロリアクターを用いて、直径130、200、360、500μmの4種類の大きさに真球をしたタンパク質「ソーマチン」の微小液滴をキャピラリー部分に数100個ずつ調製した。
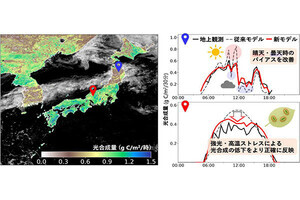
このキャピラリー部分だけを取り外し、両端を封止後、4℃の環境下に静置。数時間後、各液滴の中の結晶成長を確認したものが、画像2である。360μm以下の液滴では、液滴1個あたり、およそ1個の結晶が生じていた(画像3)。これらの結晶成長の詳細な解析がなされ、360μm以下の液滴では、たった1つの結晶が1つの液滴中に発生し、その結晶成長は拡散律速であった。

|

|
|
画像2。従来法(バッチ法)と今回の技術による単結晶のでき方の違い。今回の技術では、微小液滴の大きさが小さくなるにつれ、液滴1個あたりに生成する結晶の数が少なくなる。欄外の数値は微小液滴の体積(単位は、ナノリットル:nL) |
画像3。大きさの異なる微小液滴内に生じた結晶の個数。結晶の個数は「平均±標準偏差」で表記している |
微小液滴内では内部対流が抑えられ溶解しているタンパク質の移動は「単純拡散」(物質が自発的に散らばり広がっていく現象のこと)だけであること、1つの液滴中に1個の結晶が生じ、拡散律速によって成長し結晶となること、の2点を基に理論的な検討を行い、1個の結晶を得るために適した液滴サイズを求める計算式を得た。
この理論的検討では、液滴の中心に結晶が生じると仮定し、「フィックの第一法則」を用いた物質収支式を立て、それを解くために前述の結果を基とした近似式などを導入した。フィックの第一法則とは、フィックによって提唱された拡散に関する法則の1つであり、濃度が変化しない場合に適用される。今回の研究では、結晶成長のごく初期以外は、この法則で近似できると仮定された。
その結果、あるサイズより小さい液滴では、1個の液滴中に1個の単結晶が成長するという結論を得た。そのサイズRc(半径)は、下記の式(画像4)で示される。
ここで、qは結晶成長によって溶液中からタンパク質が減っていく速度、C0はタンパク質の初期濃度、Dはタンパク質の拡散係数である。この式はタンパク質に限らず、結晶化したい物質の拡散係数と初期濃度、結晶化に要する大まかな時間が分かれば、汎用的に適用できる。

|
|
画像4。半径Rcを求める公式 |
この式に、ソーマチンの結晶成長実験の条件を代入したところ、表1で示した結果とおおむね一致した。ただし厳密には、サイズの計算値は、実験データより若干大きめであったが、これは、結晶がいつも液滴の中心に生じるなどの計算を簡略にするための仮定と実際の結晶成長との違いによるものだ。
今回の技術による単結晶調製では、最初に1個の結晶核が発生した後、結晶が成長するにつれ、その結晶の周辺部においてタンパク質濃度が薄くなるという濃度勾配が生じ、制御された「過飽和」(溶液が、本来の溶解度を超えて溶質を含んでいる状態のこと)が解消されると考えられる。
逆に、上記サイズを超えた液滴では、タンパク質の高濃度部分が成長中の結晶から離れた場所に維持され、結果として2個目の結晶核が発生し結晶成長する可能性が生じるという。
研究グループは今回開発した技術に対し、これまでは微小重力下でなければ実現しないと考えられてきた拡散律速による結晶成長を今回の技術や理論式によって達成できたことから、タンパク質の立体構造解析をより簡単にし、これまで結晶化自体が難しかったタンパク質の立体構造解析にも道を拓き、生命現象の分子レベルでの理解や医薬品開発などの産業応用への貢献が期待されるとしている。
また研究グループは今後、さまざまなタンパク質、特に針状の結晶となるものなど、従来法では難しかったタンパク質の結晶化を行っていくとしている。さらにキャピラリー中の微小液滴内に単結晶が得られることから、そのまま結晶を取り出さずにX線回折測定ができるため、実際にそのような測定を行う予定であるという。
そして今回の技術は、結晶の成長過程の制御により結晶1個だけを生成させるものだが、何らかの結晶核発生制御技術と組み合わせると、より短時間により計算値に近い大きさの液滴で結晶が得られると期待され、そのような技術との融合による高度化を目指すとも述べている。