岡山大学は5月17日、就実大学との共同研究により、C型肝炎ウイルス(HCV)感染により引き起こされるC型慢性肝炎の治療薬として使用されている核酸アナログである「リバビリン」の作用機序の解明に取り組み、リバビリンの抗HCV活性を決定する宿主遺伝子の同定に成功し、またその宿主遺伝子が発現する際に特殊な機構が働いていることも明らかにした。
成果は、岡山大 医歯薬学総合研究科 腫瘍ウイルス学分野の加藤宣之教授らの研究チームによるもの。研究の詳細な内容は、米国東部時間3月26日付けで米国肝臓専門誌「Hepatology」電子版に掲載された。
今回同定した宿主因子は「アデノシンキナーゼという核酸代謝酵素」の1種で、リバビリンをリン酸化する機能を持つ。そしてリン酸化されたリバビリンは「イノシン」→「リン酸脱水素酵素」を阻害して、「GTP(グアノシン三リン酸)」の細胞内濃度を急速に下げる。これによりHCV遺伝子の複製が低下するので、リバビリンの抗HCV活性が発揮されるというわけだ。
今回の研究により、リバビリンの抗HCV活性がアデノシンキナーゼ遺伝子の発現レベルに依存していることが明らかになった。さらに、アデノシンキナーゼ・メッセンジャーRNAの翻訳は通常の翻訳機構とは異なり、「IRES(internal ribosome entry site)」という特殊な翻訳機構で行われていることも判明したのである。
これら一連の研究成果は、2009年に研究チームが独自に見出したHCV複製を許容する新しいヒト培養細胞(欧米特許審査中)を用いることにより得られたという。この新しいヒト培養細胞は、これまで汎用されて来た培養細胞とは異なりリバビリンに高感受性を示したことから、これまで困難であったリバビリンの作用機序の解明を行うことができた。
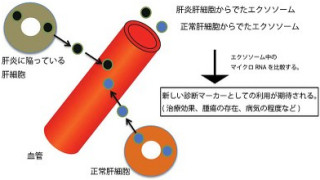
アデノシンキナーゼの発現レベルを知ることにより、肝炎治療における投与量の決定や治療効果の予測、さらには貧血などの副作用のコントロールに役立つことが期待されるという。また、アデノシンキナーゼ遺伝子の発現増強剤やアデノシンキナーゼの活性化剤を見出すことができれば、リバビリンの抗HCV活性をさらに高めて治療効果を上げることが期待されるとしている。
さらに、今回の研究成果により得られた宿主遺伝子の発現調節を人為的に行うことができれば、リバビリンの抗ウイルス作用を高めることや貧血等の副作用の軽減が可能になるものと期待されるという。