東京大学は、遺伝子群「HMGA」を発現させることで出生以降の神経幹細胞でもニューロンを産み出すことができるようになる、すなわち神経幹細胞を若返らせることができることを発見し、その若返りは培養皿上だけでなく、生体の脳においても起こり得ることを示したと発表した。
成果は、東大 分子細胞生物学研究所の後藤由季子教授、同岸雄介助教、東大大学院 新領域創成科学研究科 博士課程3年の藤井佑紀氏らの研究グループによるもの。研究の詳細な内容は、7月16日付けで「Nature Neuroscience」オンライン版に掲載された。
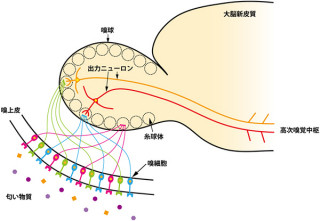
大脳は哺乳類の高度な生命機能を司る器官で、脳内ではニューロンにより複雑なネットワークが作られている。このニューロン及びそれを支持する「グリア細胞」は、神経幹細胞と呼ばれる細胞から産生される。
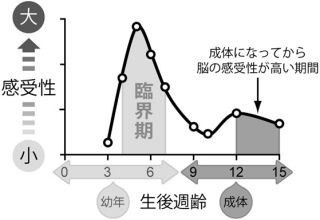
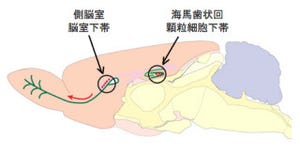
脳内ネットワークの素子であるニューロンは主に胎児期に産生され、出生以降の神経幹細胞はほとんどニューロンを産生できなくなってしまう。しかしながら、神経幹細胞がニューロンを産生する能力を失う原因についてはわかっていなかった。
今回のマウスを用いた研究では、非ヒストン性のクロマチンタンパク質をコードする遺伝子群HMGAが神経幹細胞のニューロンを産み出す能力に重要であることが見出された。胎児期の神経幹細胞においてHMGAの発現を低下させると、その神経幹細胞はニューロンを産生することができなくなったのである。
HMGAは胎児期の神経幹細胞では発現が高く、出生以降になると発現が低下するという特性を持つ。つまりこの結果は、HMGAの発現が高いことが神経幹細胞のニューロンを産み出す能力に重要であることを示唆しているというわけだ。
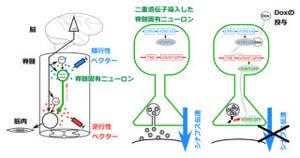
また重要なこととして、ニューロンを産み出すことができなくなった出生以降の神経幹細胞に対して、生体内においてHMGAを過剰発現したところ、その神経幹細胞が再びニューロンを産み出すことができるようになることも確認された。すなわち、これはHMGAの過剰発現によって神経幹細胞が若返ったことを示唆している。
実際に神経幹細胞を若返らせてニューロンを補うといった再生医療を実現するには、HMGAがどのようにして神経幹細胞を若返らせているのか、そのメカニズムを知ることが非常に重要だ。
今回の研究では、そのメカニズムを解明する端緒となる現象も発見された。それは、HMGAが「クロマチン」の状態をゲノム全体で制御している可能性である。実際に、胎児期の神経幹細胞では、出生以降の神経幹細胞に比べて遺伝情報を格納しているゲノムの状態があまり凝集していない、「ゆるい」状態であることが今回判明した。
さらに、その「ゆるい」状態にはHMGA遺伝子群の発現が高いことが重要であることも見出されたのである。これらの結果は、HMGA遺伝子群がゲノムの状態を「ゆるく」することが神経幹細胞のニューロンを産み出す能力に重要である可能性を示唆しているという。
今回の研究では、神経幹細胞の若返りを誘導する因子の発見に成功した。近年、細胞の若返り因子は多数発見されているが、今回の研究のように生体内での若返りが発見された例は、世界で初めてであると考えられるという。
また、生体内の神経幹細胞を若返らせてニューロンを産生させることを通じて、ニューロンの喪失、あるいは機能不全を原因とした神経疾患を治療できる可能性を示唆していると、研究グループはコメントしている。