千葉大学と理化学研究所(理研)は3月13日、植物が生産する薬用アルカロイドのカギとなる酵素遺伝子を発見したと発表した。成果は、千葉大大学院薬学研究院の山崎真巳准教授、ソムヌク・ブンスパ研究員、齊藤和季教授らと、理研植物科学研究センターの共同研究グループによるもの。詳細な研究内容は、米科学誌「The Plant Cell」への掲載に先立ち、近日中にオンライン版に掲載される予定だ。
植物は、生体防御のために多様な二次代謝成分を作っている。植物の苦味やえぐ味、渋味はこの二次代謝成分によるもので、中でも苦味成分の代表とされるのがアルカロイドだ。アルカロイドは窒素原子を含む化合物の総称で、その多くはアミノ酸から生合成されている。
マメ科「ルピナス」属の植物は、アミノ酸の「リジン」から「キノリチジンアルカロイド」を生産するが、大きな豆(=種子)をつけるので世界各地で食料や飼料として利用されてきた。
ただし、食料や飼料として利用するには苦いと都合が悪いので、アルカロイドを含む苦い品種(ビター種)に対して、育種によってアルカロイドを含まない品種(スイート品種)が作られてきた経緯がある。これは多くの作物でも行われてきたことだ。こうして育種されたスイート品種は作物として優良だが、反面、虫害を受けやすいという弱点を持っている(画像1)。
ルピナスのほか、漢方などに使われる生薬「苦参(クジン)」の基原植物である「クララ」などもキノリチジンアルカロイドを含む植物だ。これらは「苦参」の薬用成分とされている。
このように、キノリチジンアルカロイドは広範な生理活性を有しているが、これらがどのように前駆体であるアミノ酸から生産されるのか、その仕組みは長い間の謎だった。
そこで研究グループが実施することにしたのが、マメ科ルピナス属植物などでアミノ酸からアルカロイドが生産される最初のステップを触媒する酵素である「リジン脱炭酸酵素」の遺伝子と、その遺伝子産物の機能の解析である。
まず、マメ科の植物である「ホソバルピナス」のアルカロイドを含むビター品種と、アルカロイドを含まないスイート品種を比較することにより、ビター品種に特異的に発現する遺伝子を網羅的にプロファイリングした。その中に、「オルニチン脱炭酸酵素」に類似した配列を有するホモログ遺伝子が含まれていたというわけだ。
一般的に、植物のオルニチン脱炭酸酵素は副反応としてわずかにリジンを脱炭酸する。調査の結果、このホソバルピナスの酵素は、ほかのオルニチン脱炭酸酵素に比べてはるかに効率よくリジンを脱炭酸し、アルカロイド生合成の前駆体である「カダベリン」を生成することがわかった。新規の「リジン脱炭酸酵素」であることが示されたのである。
また、この新酵素の遺伝子をシロイヌナズナやタバコで発現させると、これらのトランスジェニック植物はカダベリンやカダベリンに由来するアルカロイドを多く生産するようになることがわかり、この遺伝子が植物体内でリジンを脱炭酸してカダベリンを合成し、リジンを前駆体とするアルカロイド生合成に関与することが示された次第だ。
このホソバルピナスからの新酵素の触媒的特性は、この酵素の活性中心の1つの「アミノ酸残基」が異なることによることが明らかになった。通常のオルニチン脱炭酸酵素では、基質結合部位の隣のアミノ酸残基は「ヒスチジン」だが、ホソバルピナスの酵素では「フェニルアラニン」に置換していたのである。
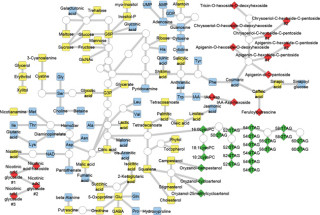
分子モデリングの結果、このアミノ残基の違いによって活性部位ポケットの「くぼみ」の大きさが変化し、オルニチンより炭素鎖が1つ分だけ長いリジンが酵素に取り込まれて、脱炭酸されることが示された(画像2・3)。
ホソバルピナスのほかにも「クララ」、「イヌクララ」、「センダイハギ」、「ムラサキセンダイハギ」など、キノリチジンアルカロイドを含む薬用植物からもこの酵素遺伝子を単離し、アミノ酸配列と酵素活性が調べられた。
すると、やはりリジン脱炭酸活性を有し、また同じ位置のアミノ酸残基がホソバルピナスの酵素と共通してフェニルアラニンに置換していることが明らかになったのである。
このように複数種でアルカロイド生産と酵素のアミノ酸置換と触媒特性が一致していることから、この酵素の触媒的特性により、これらの植物はアルカロイドを生産するようになったと推測された。
植物を初めとする天然生物資源から多くの新薬が生み出されており、さらにこの豊富な天然資源をエンジニアリングすることで、より有効な新薬が得られることが期待されている状況だ。
今回の研究では、リジン由来アルカロイド生合成の第1段階の重要な酵素遺伝子を同定することに成功した。この遺伝子を応用することで、天然からは未だ得られていないが、新しい構造と生物活性を有する新しいアルカロイドを遺伝子組換え植物によって生産できるようになることも期待されているという。
また、キノリチジンアルカロイドのほかにもリジンを原料として生産される多様な植物アルカロイドが知られており、それらの中にはアルツハイマー治療薬などに医薬品資源として重要な化合物もある。
研究グループは、今回の成果によって植物におけるアルカロイド生産の分子基盤が明らかになったことで、将来、医薬品や農薬など生理活性物質の安定生産やアルカロイド創薬への展開といった応用が期待されるとコメントした。