名古屋大学(名大)は5月7日、米SRI Internationalとの共同研究により、睡眠障害の1種である「ナルコレプシー」の新たなモデルマウスの作製に成功し、新たな治療薬の作用を確認したと発表した。
成果は、名大 環境医学研究所 ストレス受容・応答研究部門 神経系分野IIの山中章弘 教授、SRI InternationalのThomas Kilduff博士らの国際共同研究チームによるもの。研究の詳細な内容は、現地時間5月7日付けで英科学電子ジャーナル「Published by the Society for Neuroscience」に掲載された。
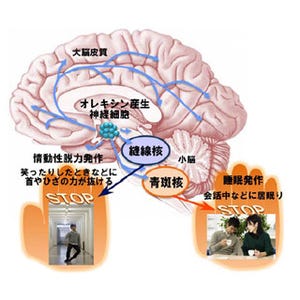
ナルコレプシーは2000人に1人の有病率とされ、その特徴は何をしていても眠ってしまうほどの日中の耐えがたい眠気、寝続けることができない睡眠覚醒の分断化、寝入りばなに夢を見るために現実世界と区別がつかない入眠時幻覚、喜んだり笑ったりなどの情動変化により全身の筋肉が脱力して倒れる「情動脱力発作」などを主な症状とする睡眠障害の1種だ。
覚醒の維持に重要な役割を担う神経ペプチド「オレキシン」を産生し、視床下部に少数存在する「オレキシン神経細胞」が、何らかの原因によって脱落する(なくなってしまう)ことによって発症し、思春期または成人期初期に発症しやすいことがわかっている。
しかし大きな問題があり、確定診断までに平均して約10年もかかるため、発症初期からの症状変化を調べることができないのが現状だ。そのため、ナルコレプシーの研究にはモデル動物が用いられているのだが、従来のモデル動物は生後間もなくオレキシン神経細胞が消失するように遺伝子改変されたマウスであり、思春期または成人期初期に好発するヒトのナルコレプシーとは異なっていたのである。
そこで今回の研究では、任意のタイミングで目的遺伝子の発現を制御できる遺伝子発現のスイッチを用いて、オレキシン神経細胞だけで細胞死を起こさせる技術を開発。遺伝子発現のスイッチをオンにすると、オレキシン神経細胞において、タンパク質合成を阻害して細胞死を誘導する「ジフテリア毒素A断片」の生産が始まり、同細胞だけが死滅するという仕組みだ(ジフテリア毒素にはB断片もあり、A断片はB断片の細胞内への進入手助けするのが役割で、A断片だけでは発現細胞において細胞死を誘導するのみで、周囲の細胞には影響を与える心配がない)。なお、今回の技術はスイッチをオフにして細胞死を任意のタイミングで止めることも可能である。
この遺伝子発現システムの制御は、遺伝子発現のスイッチのオン・オフはエサを替えることで行われる仕組みだ。具体的には、特殊なエサが与えられている状態ではスイッチが入らず、オレキシン神経細胞は正常に保たれる。しかし普通のエサに替えると毒素の発現が誘導され、オレキシン神経細胞が細胞死していくというわけだ。
実験ではこの遺伝子改変マウスを10週齢まで特殊なエサで飼育し、その後、普通のエサに置き換えてオレキシン神経細胞死を誘導し、残存するオレキシン神経細胞数の観察が行われた。その結果、計画通りに特殊なエサが与えられている状態ではまったく正常だったが、普通のエサに交換するだけでオレキシン神経細胞の数が急速に減少したのである。
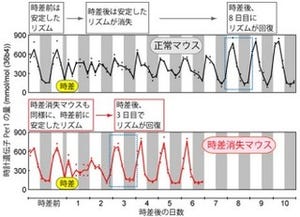
そして、そのオレキシン細胞の数が急速に減少していくタイミングで睡眠覚醒パターンの解析が行われた。すると、普通のエサにして1週間後には85%以上のオレキシン神経細胞が死滅し、睡眠覚醒の分断化がスタート。2週間後には95%が死滅し、この時に初めて情動脱力発作が現れることが確認された。さらに死滅する割合が95%以上に至ると、睡眠覚醒の分断化が顕著となり、情動脱力発作の頻度も上昇したのである(画像)。
今回開発された技術は任意のタイミングでオレキシン神経細胞を死滅させられるため、ヒトのナルコレプシー患者同様に、思春期や成人期初期のタイミングで好発するナルコレプシーを再現できるようになったのが大きな特徴だ。また、ヒトのナルコレプシーは、日中の強い眠気をのみという患者から、情動脱力発作を起こす患者まで症状にバラツキがあるが、今回の技術は任意のタイミングでオレキシン神経細胞除去の開始・停止ができることから、オーダーメイド的に各患者の症状に近いマウスを作製することも可能だという。
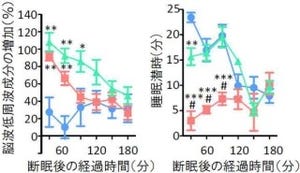
また、今回の新たなモデルマウスを用いて、ナルコレプシー治療薬となり得る薬の治療効果の検討も行われた。現在、筋痙縮の治療薬として「R-バクロフェン」が、ナルコレプシーの治療薬としては「GHB(γ-ヒドロキシブチレート)」が使われているが、それらが投与されたところ、R-バクロフェンにより睡眠覚醒の分断化が改善され、情動脱力発作の回数も減少することが確認されたのである。R-バクロフェンはGHBよりも治療効果が高いこともわかったという。
今回の成果により、これまでは不明だった、オレキシン神経細胞の数とナルコレプシーの発症・症状の程度の関係を明らかにすることが成功した形だ。研究チームは今後も、さまざまな症状を呈するマウスを作製して治療薬を開発していくことで、症状に個人差があるナルコレプシーの治療に大いに貢献できると考えているとした。さらに、オレキシン神経細胞は睡眠覚醒の役割のみでなく、不安行動や依存などにも深く関わっている神経であることから、今回のあたらなモデルマウスを用いることで、オレキシン神経細胞に関連するさまざまな生理的役割を明らかにできるとしている。