京都大学は1月20日、Tリンパ球活性化により起こるダイナミックな酸性糖「シアル酸」を含む「糖鎖」の変化は、シアル酸結合タンパク質を介した免疫細胞同士の結合に変化をもたらす仕組みであること、つまり免疫系における細胞結合のための分子スイッチとなることを明らかにしたと発表した。
成果は、京大 医学研究科の竹松弘 准教授、同・大学 生命科学研究科の内藤裕子 助教(当時)らの研究チームによるもの。研究の詳細な内容は、2013年12月2日付けで「Journal of Biological Chemistry」電子版に掲載された。
糖といえばグルコースを代表とする地球上の生命のエネルギー源であるが、生体は、糖を使ってポリマーを形成し、エネルギー源以外の機能も糖に付与している。最も代表的な例がグルコースのポリマーだ。そのポリマーにおける結合様式が変わると、栄養源となるデンプンと同様の組成で、セルロース繊維を構成するというわけだ。
細胞の表面は糖鎖で覆われているが、その糖鎖の末端を占めるのがシアル酸だ。「カルボキシル基」を持つ酸性の単糖の1種。分子としては「ノイラミン酸骨格」を持つ。細胞はこのシアル酸を介してほかの細胞や分子との認識を行っており、このシアル酸を介した分子間の認識(結合)がさまざまな細胞の機能に重要な役割を果たすことが知られている。またシアル酸はその末端での局在から、インフルエンザウイルスといった病原体の標的となることも多い。
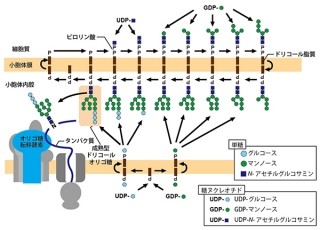
免疫系のリンパ球もこのような分子間認識を介して制御されていることが考えられるが、リンパ球が活性化すると、複数あるシアル酸の分子種の内、主要な分子種が「N-グリコリル(N-グリコリルノイラミン酸)型」から「N-アセチル(N-アセチルノイラミン酸)型」へと変換されることが報告されていた(画像1)。シアル酸分子内に複数存在するヒドロキシル基(水酸基)が修飾され、C5位に着目すると、これらの分子種がわかる。つまり、T細胞は活性化されてもシアル酸は持ち続けるが、その種類を変化させるというわけだ。
細胞表面の糖鎖は「第3の生命鎖」、「細胞の顔」などとも称され、異なる細胞は異なる糖鎖を発現することが広く知られているが、その一方で、これら糖鎖の違いがどのような認識分子により認識されるのかなど、その分子機構については未知な部分が多く、生命科学分野におけるフォロンティア領域であるとも考えられるという。そこで、今回、活性化したTリンパ球におけるシアル酸分子種の変化に注目し、その免疫応答における意義の解明が試みられたのである。
まず研究チームは免疫応答において中心的な役割を果たすTリンパ球に着目し、マウス活性化Tリンパ球においてシアル酸分子種の変化を起こすメカニズムから調べることにした。その結果解明したのが、Tリンパ球はN-アセチル型からN-グリコリル型を作る酵素「CMAH」の遺伝子発現を抑制しているという事実だ。
また、シアル酸分子種の変化はシアル酸結合タンパク質である「シグレックファミリーレクチン」からの認識を変化させることも判明。シグレックファミリーはシアル酸の修飾や、結合様式の違いを認識でき、細胞内でのシグナル伝達経路を制御することのできる分子群であると考えられる。その一方で、細胞と細胞の結合を媒介する細胞接着分子としても働く。そして活性化Tリンパ球はBリンパ球上の分子「CD22」からの認識を逃れると共に、同じく免疫細胞のマクロファージ上のレクチン「シアロアドヘジン」との結合性を上昇させていたのである。
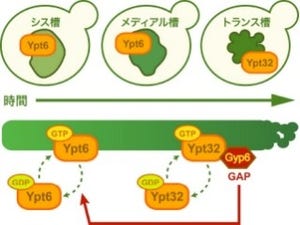
N-グリコリル型を作れないCMAH遺伝子欠損マウスを用いてTリンパ球の活性化を調べると、CMAH欠損マウスではTリンパ球の活性化が亢進していることが確認された。つまり、N-グリコリル型のシアル酸は活性化を抑制するが、Tリンパ球の活性化はN-グリコリル型のシアル酸の発現を抑制しており、シアル酸とTリンパ球活性化の関係を考えると、両者はポジティブフィードバックの関係にあったのである(画像2)。
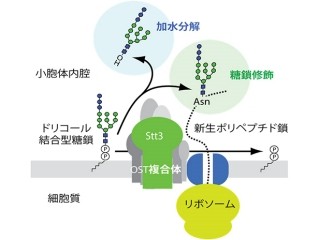
また、N-グリコリル型の抑制が起こっていない活性化前のTリンパ球では、活性型モデルBリンパ球とのCD22を介した結合が亢進しており、抗原非特異的なTリンパ球とBリンパ球の結合を起こすことがわかった。Bリンパ球が活性化する場であり、Tリンパ球が認識する抗原特異的にBリンパ球の活性化を助ける「胚中心」において、活性化リンパ球におけるシアル酸分子種の制御は、本来、応答する抗原を介して結合するべきリンパ球同士の認識を可能にしていることが明らかとなったのである(画像3)。
よって、今回新たに作成されたN-グリコリル型を抑制できないCMAH遺伝子トランスジェニックマウスでは、マクロファージとの結合が抑制されることで、細胞障害性Tリンパ球の活性化が亢進することが示唆された。
|
|
|
|
画像2(左):。Tリンパ球の活性化に伴うシアル酸分子種の変換を介したポジティブフィードバック様の制御。画像3(右):非活性化時には、Bリンパ球上のCD22は細胞外とアクセスできないが、活性化に伴い、Tリンパ球上の糖鎖と結合することができるようになる。しかし、活性化Tリンパ球もN-グリコリル型のシアル酸をN-アセチル型に変換することで、抗原(黄色)を介したT細胞とB細胞の結合を起こす |
|
今回の研究結果から、マウス免疫系は抗原を介したリンパ球間の結合を可能とするため、発現するシアル酸分子種をうまく制御していることが考えられるとした。これらシアル酸を含む糖鎖は細胞の外側に存在するため、免疫系におけるシアル酸とシアル酸結合タンパク質との結合を人為的に制御することで、リンパ球が結合する細胞を制御できることが考えられ、これを介して、免疫応答を人為的に制御できる可能性が考えられるとした。
ヒトではCMAH遺伝子が欠損しており、N-グリコリル型のシアル酸を生合成できないと共に、ヒトは上述のシアル酸分子種を介したリンパ球の活性化を制御できないとする。このCMAH遺伝子欠損はチンパンジーとの分岐後に起こったもので、ヒトに特徴的な性質だ。
その事実から、今後は、CHAH遺伝子欠損マウスをよりヒトの状態を反映できるモデルマウスとしてとらえ、ヒトの免疫制御に結びつける研究を行っていく予定とした。