大阪大学(阪大)は、緑膿菌および大腸菌の主な多剤排出タンパク質の阻害剤の結合構造の決定に成功したことを発表した。
同成果は、同大産業科学研究所の山口明人 特任教授らによるもの。詳細は米国科学誌「Nature」に掲載された。
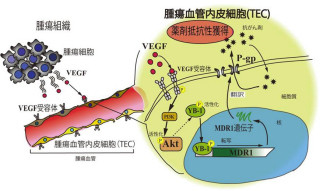
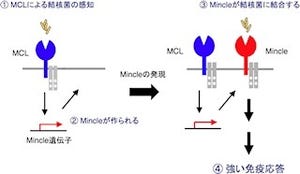
細菌が薬物に対する耐性を獲得する主な原因である多剤(異物)排出タンパク質は生物の細胞膜上に広く存在しているが、病原細菌などの細胞膜上で増加すると、多剤耐性を引き起こしてしまうことから、各所で多剤排出タンパク質の阻害剤の開発に向けた研究が進めらられているが、いまだに臨床的に有効な阻害剤は得られていない。
中でも多剤耐性のある緑膿菌には有効な治療薬がまったく存在しない状況である。例えばピリドピリミジン誘導体「ABI-PP」は、大腸菌の多剤排出タンパク質「AcrB」を阻害するため、緑膿菌の多剤排出タンパク質「MexB」の特異的阻害剤となるが、多剤耐性緑膿菌のもう1つの有力な原因である多剤排出タンパク質「MexY」をまったく阻害できないため、多剤耐性緑膿菌感染症の治療薬として使用することができなかった。
今回の研究は、多剤排出タンパク質とその阻害剤の選択的な結合構造を明らかにすることで、AcrB、MexB、MexYを阻害する多剤耐性感染症治療薬を、タンパク質立体構造情報に基づく薬剤設計手法「SBDD(Structure-Based Drug Design)」によって分子設計することを可能としたもので、これにより、多剤耐性緑膿菌感染症に有効な治療薬の開発が期待できるようになると研究グループでは説明している。