東京大学(東大)は、独自開発による手法を用いることで高分子に固定化することで無害化に成功した環境に優しい「オスミウム触媒(PI Os)」を開発し、抗がん剤の中間体合成を行ったことを発表した。同成果は同大大学院理学系研究科の小林修教授、東京大学大学院薬学系研究科、名古屋大学(大学院工学研究科、エコトピア科学研究所)らの研究グループによるもので、「RSC Advances」オンライン版に掲載された。
現代では、環境への負荷を減らし社会の持続性を重視するグリーン・サステイナブル・ケミストリーの観点から、例え高活性であっても毒性の高い試薬や触媒の使用は避けられる傾向にある。こうした高活性だが毒性の高い試薬や触媒の使用例として、鉛や水銀由来の試薬や触媒、四価の有機スズなどがあるが、四酸化オスミウムもアルケンのジヒドロキシル化に用いられる有用な触媒であるものの、毒性が高く、かつ揮発性であるために使用が避けられるものとなっている。この四酸化オスミウムはキラル配位子と組み合わせることで触媒的不斉ジヒドロキシル化反応が可能なため、光学活性ジオールを効率的に供給することができ、天然物や医薬品、ファインケミカルなどの合成に広く用いられるが、高い毒性と反応後のオスミウムの分離や回収の困難さから、工業化に成功した例はほとんどない。
すでにいくつかの研究グループによりキラル配位子の担体への固定化が検討されてきたが、オスミウムの回収や再使用は困難であったが、研究グループでは、これまでに、同時に開発した高分子を用いたマイクロカプセル化法により四酸化オスミウムを高分子に固定化することで、オスミウムが高分子から漏れ出すことなく触媒的不斉ジヒドロキシル化反応が高い収率および選択性で進行することを明らかにしていた。しかし使用できる溶媒の種類が限られており、他の研究グループが種々の固定化法を検討しているが、従来同様の問題が発生することから、工業的利用を含むスケールアップ合成に関する報告例はほぼなかった。
そこで研究グループは今回、毒性および揮発性の無い高分子固定化オスミウム触媒(polymer-incarcerated osmium:PI Os)を新たに開発し、アルケンの触媒的不斉ジヒドロキシル化反応において活性を失うことなく回収および再使用が可能であること示した。
具体的には、この新たなオスミウム触媒は、独自開発の「高分子カルセランド法(polymer-incarcerated method:PI法)」に基づいて調製された。PI法はマイクロカプセル化と架橋反応の2つのプロセスから構成されている。マイクロカプセル化法はもともと高分子のベンゼン環との相互作用により金属ナノクラスターを高分子内に安定に保持する方法として開発されたものだが、その欠点は、溶媒により高分子が溶解して回収や再使用が困難になる場合があることであり、今回、この問題を解決するために架橋反応を行うことで耐溶剤性を高め、かつ触媒が高分子内に物理的にも保持されて漏れ出しを防ぐようにした。
今回の研究では、四酸化オスミウムを高分子の溶液に加えて72時間撹拌し、さらにヘキサンを加えることで黒色のマイクロカプセル化オスミウム(MC Os)を生成。一晩撹拌した後に溶媒を除去し、洗浄、乾燥を行った後、加熱して架橋反応を行い、濾過、洗浄を行い、PI Osを調製した。こうして得られたPI Osはほとんどの有機溶媒と水に不溶であることが確認された。
研究では3種類の高分子を用いてPI Os A~Cを調製。これらのPI Osは黒色粉末で空気中において数カ月保存しても安定であることが確認されたほか、四酸化オスミウムとの揮発性の比較実験においてオスミウム成分の揮発は観察されなかったという。
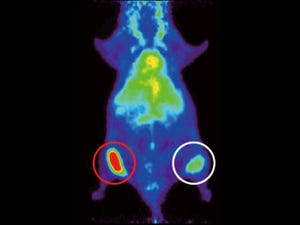
また、マウスを用いた急性毒性試験において、PI Os Cを投与した5匹のマウスは特に障害なく投与後一週間の生存が確認されたほか、マウス体内の器官を調べたところPI Os C投与の場合にオスミウムは検出されず、器官への吸収が起きていないことが明らかになった。
さらにモデル基質としてα-メチルスチレンを選び、PI Os A~Cを用いて不斉ジヒドロキシル化反応を行ったところ、良好な収率および選択性で反応が進行することを確認。PI Os BおよびCではオスミウムの漏れ出しがほとんど無く、Cの高分子担体が調製容易であることからPI Os Cを今後用いることとし、他のさまざまな種類のアルケンを用いた場合にも良好な結果が得られたほか、PI Os Cは活性を失うことなく回収および再使用が可能であることも確認された。
研究では、抗がん剤であるカンプトテシンの鍵中間体の合成に同方法の適用も行っている。
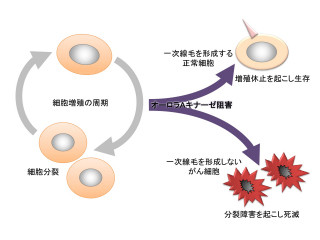
カンプトテシンはDNAトポイソメラーゼIを阻害する細胞毒性のあるキノリンアルカロイドで、類縁体であるトポテカンとイリノテカンはがん治療に用いられているが、反応条件の最適化を行った後、原料を1mol(190g)用いて工業化を視野に入れたスケールアップ条件での反応を行った結果、97%(234g)、86% eeと高い収率およびエナンチオ選択性で生成物を得ることができたとするほかPI Os Cは濾過によりほぼ定量的(97%)に回収することができたという。
今回の成果は、毒性や揮発性のある触媒を独自の手法で高分子に固定化することで無害化し、工業化の可能性を実証した点においてグリーン・サステイナブル・ケミストリーの観点から重要な成果であり、このジヒドロキシル化プロセスの実用化により化学品製造プロセスが環境にやさしくかつ効率的なプロセスに改善されていくことが期待できるようになるという。また、今回開発されたPI Osは、大きな工業スケールでのプロセスにも適用できることが予想されるほか、PI法はオスミウム以外の高活性ながら毒性や揮発性のために使用されることが少ない種類の試薬や触媒に対しても適用できる可能性があり、今後の研究の進展が期待できると研究グループではコメントしている。