東京大学(東大)医科学研究所の中内啓光 教授と科学技術振興機構(JST)戦略的創造研究推進事業 ERATO型研究「中内幹細胞制御プロジェクト」の山崎聡 研究員らの研究グループは、生体内で血液細胞のもととなる「造血幹細胞」の能力の維持に必要と考えられる「冬眠状態」に、神経細胞の一種であるグリア細胞が重要な役割を果たしていることを明らかにした。同成果は、2011年11月23日(米国東部時間)発行の米国科学雑誌「Cell」に掲載される。
血液は人の体重の約8%を占め、全身に酸素を運ぶ赤血球、感染防御に働く白血球など、さまざまな血液細胞が存在するが、どの血液細胞も寿命が短いため、常に供給し続けなければならない。こうした各種の細胞を作り出す源(種)になる細胞が「造血幹細胞」と呼ばれる細胞だ。造血幹細胞は自分自身を複製する能力と、さまざまな血液細胞を作り出すことができる能力を兼ね備えており、生涯にわたって血液細胞を供給し続ける。
臨床の現場で白血病の治療方法として行われる骨髄移植は、造血幹細胞の再生能力の高い性質を利用した、造血幹細胞の移植による造血系の再生であるなど、生涯にわたり造血幹細胞がさまざまな血液細胞を正常に供給し続けるためには、その種となる造血幹細胞のゲノムが突然変異を起こさないための工夫や、細胞が尽きないような工夫が必要となる。その工夫の1つが造血幹細胞の冬眠で、冬眠状態で骨髄ニッチと呼ばれる隠れ家でひそかに生き続けていると考えられている。しかし、骨髄のどの場所(ニッチ)に造血幹細胞が存在しているか、そのニッチがどのようなメカニズムで造血幹細胞を冬眠状態にしているのか、ほとんど分かってはいなかった。
今回の研究は、骨髄中に存在する造血幹細胞の冬眠の維持に関わるシグナルを手がかりに、ニッチを構成する細胞を明らかにすることを目指して行われた。
まず、研究では造血幹細胞の冬眠状態に着目し、「骨髄ニッチには造血幹細胞を冬眠させる働きがある」という仮説をたて、造血幹細胞の細胞分裂を抑制する分子をスクリーニングした。その結果、サイトカインというたんぱく質の一種である「TGF-β」が造血幹細胞の分裂を抑制することを発見したほか、TGF-βの受容体を欠損させたマウス(TGF-βが結合できず、TGF-βが機能しないマウス)を使い造血幹細胞の機能を解析したところ、通常のマウスと比較してTGF-β受容体欠損マウスの造血幹細胞は冬眠状態の造血幹細胞が少なく、その機能などが著しく低下していることが分かり、造血幹細胞におけるTGF-βの重要性が確認できたという。
この成果から、TGF-βが造血幹細胞の冬眠状態の維持に関与しているとすると、骨髄中でTGF-βを産生している場所が骨髄ニッチと考えられることとなる。詳しく調べてみた結果、造血幹細胞自身を含む多くの細胞が、骨髄中でTGF-βを産生していることが確認された。しかし、これらのTGF-βのほとんどは不活性型TGF-βで、活性型のTGF-βを発現している細胞はわずかであることが判明したことから、このTGF-β活性化のメカニズムに注目して研究をさらに進めたという。
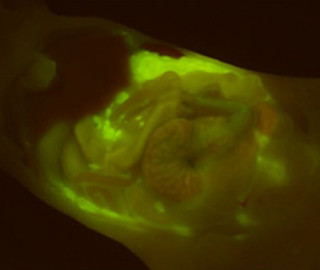
造血幹細胞の働きに重要な活性型TGF-βが骨髄の中のどこに存在しているのかを探るため、マウスの骨髄を、活性型TGF-βと特異的に反応する抗体を用いて免疫染色法で解析してみたところ、わずかに血管に似た構造をとる細胞が特異的に染色されることが判明したことから、その血管に似た細胞がどのような細胞なのかさらに解析を進めていったところ、活性型TGF-βが貯まる場所は血管細胞ではなく、血管と並行して存在する神経系の細胞であることが確認されたという。
|
|
|
骨髄内の血管と神経系細胞(骨髄組織切片を活性型TGF-β、血管細胞とそれぞれ特異的に反応する蛍光抗体で免疫染色した写真)。活性型TGF-βは赤、血管は緑、そして細胞の核は青に染まっている。骨髄内で活性型TGF-βを産生している細胞が血管と並走しているが、血管とは異なる細胞であることが分かる。また、別の解析で、活性型TGF-βを産生している細胞が神経系の細胞であることが明らかになった |
さらに詳しい解析を行った結果、この神経細胞はグリア細胞の一種である「非ミエリン髄鞘シュワン細胞(non-myelinating Schwann細胞)」であることが明らかとなった。これまで、骨髄中に存在する造血幹細胞が非常に少ないこと(3万個に1個程度の頻度で存在)が骨髄ニッチの研究を難しくしていたこともあり、研究グループでは臓器の組織切片画像を、画像解析装置の一種である「ArrayScan」を導入し、造血幹細胞が組織中のどの場所に存在するかを高速かつ客観的に解析した。その結果、多くの造血幹細胞が、活性型TGF-βを発現しているグリア細胞に寄り添って存在していることが確認できたという。 造血幹細胞と神経系細胞が同じ場所にいたからといっても、偶然近くにいるだけの可能性もあるため、造血幹細胞と神経細胞とが何らかの相互作用をしていることを確かめるため、骨髄に入り込む神経を切断してみた結果、神経を遮断した骨髄では、造血幹細胞の数が大きく減少するという現象がみられた。さらに興味深いことに、切断後は造血幹細胞が冬眠から目覚めて分裂をしていることが確認されたという。
これらの成果により、造血幹細胞の冬眠状態を維持する骨髄中のニッチを構成する細胞として、神経系細胞の一種であるグリア細胞が関与していることが明らかとなった。
|
|
|
TGF-βの活性化による造血幹細胞の冬眠状態の仕組み。造血幹細胞は骨髄中の神経系細胞と接触することにより活性型TGF-βの影響を受けて冬眠状態になる。数週間から数カ月に一度、冬眠から覚めて細胞分裂し、血液前駆細胞を供給することによりさまざまな血液細胞を供給していると考えられている |
近年、白血病幹細胞も骨髄中の造血幹細胞ニッチで冬眠状態にあることが、放射線治療や化学療法に対する抵抗性との関係から指摘されており、これが白血病再発の原因である可能性が高いと考えられている。こうした観点からも造血幹細胞ニッチに関する研究は、造血の仕組みを理解することのみならず、医学的にも重要な研究課題となってきており、今回の成果が将来、白血病再発を抑えるまったく新しい治療方法へとつながることが期待できると研究グループでは説明するほか、造血幹細胞以外にも生体内にはさまざまな幹細胞が存在しており、今回の神経系による幹細胞制御の機構はほかの幹細胞にも当てはまる可能性もあり、今後の展開が期待されるともしている。