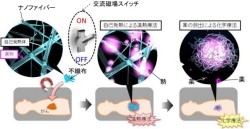
物質・材料研究機構(NIMS)は6月12日、がんの「温熱療法(ハイパーサーミア)」と化学療法(抗がん剤治療)を同時に実現させることが可能な「ナノファイバーメッシュ」(画像1)を新たに開発することに成功し、上皮性のがん細胞を効率的に「アポトーシス(プログラム細胞死)」させることに成功したと発表した。
成果は、NIMS 国際ナノアーキテクトニクス研究拠点 生体機能材料ユニットの荏原充宏MANA研究者らの研究チームによるもの。研究の詳細な内容は、日本時間6月14日付けで科学誌「Advanced Functional Materials」オンライン速報版に掲載された。
上皮性の悪性腫瘍の1つである扁平上皮がんは多くの組織で認められるがんだ。例えば、食道がんの90%以上、子宮頚部がんの80%以上、肺がんの30%以上は扁平上皮がんが占めているといわれている。治療方法は、がんの進行度によって手術、放射線療法、化学療法が3本柱となっているが、これらに加え、近年高い注目を集めているのが温熱療法だ。
温熱療法はがん細胞が正常な細胞と比べ熱に弱いことを利用して死滅させる仕組みで、抗がん剤を併用するとその効果が向上すること、疼痛緩和などの効用もわかっている。しかし、実際に温熱療法と抗がん剤投与を併用するには、独立した2つの治療法を別々に行わなければならず、これまで、同じ場所で同じタイミングで精密に制御することが困難なことが課題となっていた。
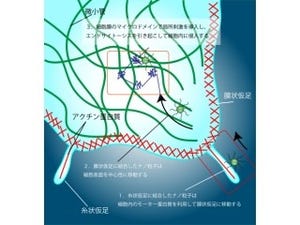
今回開発されたナノファイバーメッシュは、温度応答性高分子、磁性ナノ粒子、抗がん剤を組み合わせたハイブリッド材料が用いられており、患部に直接貼れるメッシュ状の材料である。温度応答性高分子を電解紡糸法によってナノファイバー状に加工し、不織布を作製(画像2)。この際、ファイバー内には磁性ナノ粒子が包含されているため、交流磁場の印加によって内部の磁性ナノ粒子を自己発熱させ、ファイバーを加熱することに成功した(画像3)。また、自己発熱で生じた熱に応答して、温度応答性高分子が脱水和するため、内部の水と共に内部の抗がん剤を外部に放出させることができるというわけだ(画像4)。これにより、上皮性悪性腫瘍に対して温熱療法と化学療法を同時に行えるようになったのである。

|

|

|
|
画像2(左):ナノファイバーメッシュのSEM(中央)およびTEM(左:bar200nm)写真。画像3(中):交流磁場のON-OFF切り替えに応答したナノファイバーメッシュの発熱挙動。画像4(右):交流磁場のON-OFF切り替えに応答したナノファイバーメッシュの膨潤・収縮変化とそれに伴う抗がん剤の放出 |
||
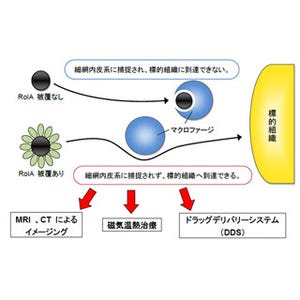
これまで開発されてきた磁性ナノ粒子を用いた磁気温熱療法の場合は、磁性ナノ粒子をそのまま体内に投与するため、患部でのハンドリングが難しい上に、磁性ナノ粒子自体の安全性が懸念されていたが、今回のナノファイバーメッシュはハンドリングしやすく、内視鏡手術などでも使用することが可能だ。また、ファイバー内の磁性粒子は安定に存在するため体内への拡散も抑えられ、磁性粒子を直接投与する方法と比べて安全性は高いと考えられる。また、ナノファイバーメッシュは、自己発熱体である磁性ナノ粒子を含んでいるため、交流磁場をかけることでファイバーを加熱でき、その生じた熱に応答して温度応答性高分子が収縮することで、内部の抗がん剤を外部に放出させる仕組みを持つ。
実際にヒトメラノーマ細胞株を用いてナノファイバーメッシュの抗がん活性が調べられたところ、交流磁場の印加によってがん細胞増殖が大幅に抑制できることが明らかとなった。磁性粒子入りファイバーおよび抗がん剤投与をそれぞれ単独に行った場合と比べ、両方を含有するナノファイバーメッシュを細胞に添加した時にもっとも高い殺傷能力(70%)が確かめられた(画像5)。
また、初期および後期のアポトーシスを調べるため、「Annexin V」および「TUNEL染色」をそれぞれ行った結果、抗がん剤と磁性粒子を含むナノファイバーメッシュを加えた際に蛍光が見られた(画像6)。これはがん細胞がアポトーシスしていることを示している。つまり、ナノファイバーメッシュをがん細胞上に乗せ、交流磁場を加えることでがん細胞を効果的にアポトーシスさせることができたというわけだ。つまり、交流磁場をかけるとがん細胞のアポトーシス誘導をON-OFF制御可能であることが明らかとなったのである。その点から、病気の治療の時空間制御(任意のタイミング・場所での薬の投与など)が求められている21世紀において、次世代医療材料の開発の大きな前進となるという。
治療技術の進歩に伴って、最近ではがん細胞が粘膜内だけにとどまる場合は、内視鏡による治療などが行えるようになってきている。すなわち、ハンドリングがしやすく、かつ、それ自体が抗がん活性を有するメッシュ状の材料の開発は、がん患者の生存率の向上のみならず、低侵襲治療法の提供にもつながると考えられるというわけだ。
例えばナノファイバーメッシュの想定される治療法としては、内視鏡でがんを取り除いた後、患部にこのメッシュを直接貼り、外から任意のタイミングで磁場をかけることで、がんを効率的に消滅させることが考えられるという。またナノファイバーメッシュは、抗がん剤や磁性粒子以外にもさまざまな物質の内包が容易に行えるため、生体透過性の高い近赤外応答材料や、そのほかの薬物との併用、さらには生分解性などを付与することでより機能的なナノファイバーメッシュの開発につながると考えられるとしている。