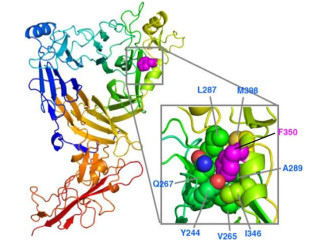
東北大学は6月4日、酸化ストレス防御機構において中心的な役割を担う転写因子「Nrf2(NF-E2 related factor2)」の「網膜神経節細胞」の死に対する関与、Nrf2活性剤の神経保護作用を明らかにしたと発表した。
成果は、東北大大学院 医学系研究科の中澤徹教授、同・丸山和一 講師、同・檜森紀子 助教、同・山本雅之教授、同・田口恵子助教らの研究チームによるもの。研究の詳細な内容は、5月30日付けで「Journal of Neurochemistry」電子版に掲載された。
緑内障は眼圧が正常値(10~21mmHg)を超えて視神経を圧迫し、視野が狭くなる疾患で、40歳以上の約5%が罹患し、日本人における失明原因の第1位となっている。現在のすべての緑内障治療は眼圧を下降させることを基本としており、それ以外の作用機序による治療法はない。
しかし、視野の保持に有用とされる30%の眼圧下降を得ても緑内障の進行が止まらない患者も約20%の割合で存在する。また、日本人は諸外国の緑内障患者と病型が異なり、全緑内障患者の約7割は眼圧が正常範囲である「正常眼圧緑内障」(正常眼圧でも視神経の委縮が進行し、視野欠損が出現する)だ。そのため、30%の眼圧下降を得ることが難しい患者もいる。従って、日本人の緑内障治療において眼圧下降のみでは限界があり、眼圧以外の危険因子へ注目し、それに対応した治療が重要となる。
緑内障の基本病態は、「視神経乳頭陥凹」に伴う網膜神経節細胞死であることから、神経保護治療に繋がる研究が着目されている。視神経乳頭陥凹とは、神経乳頭部の結合組織が減少してくぼみが拡大することだ。結果として視神経線維がだんだん委縮し、視野欠損となる。また網膜神経節細胞とは、光を感じる網膜から情報を受け取る、視神経を構成する細胞のこと。網膜神経節細胞の長い軸索が束(視神経)になって、脳へ光の情報を伝える仕組みである。
この網膜視神経を保護するためには、複雑な網膜神経節細胞死の機序を細胞レベルで解明することが必須だ。眼圧以外の因子の中で、網膜神経節細胞死に酸化ストレスが関与すると考えられており、近年、酸化ストレスセンサとして「Keap1-Nrf2システム」が重要であることが報告された。非ストレス環境下ではNrf2活性は最小限に抑制されているが、酸化ストレスに暴露されるとKeap1によるNrf2の結合が減弱し、Nrf2は核に蓄積し生体防御遺伝子の発現が亢進されるというものである。
そこで今回の研究では、「軸索挫滅」(視神経を機械的に圧迫して破壊する、緑内障の病態モデル)によってNrf2ノックアウトマウス(Nrf2KO)の緑内障動物モデル(酸化ストレスに対して脆弱なマウス)を作成し、Nrf2の網膜神経節細胞死に対する関与の解析が行われた。
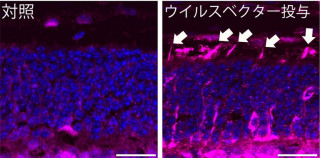
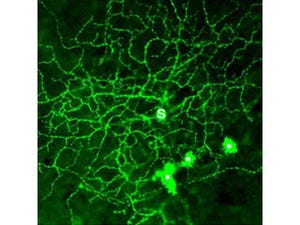
「セルソーター」によって分取した正常時網膜神経節細胞において、Nrf2とKeap1のメッセンジャーRNA(mRNA)が発現していることが判明(画像1~3)。無処置の神経節細胞密度は2群(野生型とNrf2KO群)で差が認められなかったが、軸索挫滅7日後の神経節細胞密度はNrf2KO群にて有意に減少していることがわかった(画像4・5)。

|

|
|
画像4(左)・5。無処置対照の網膜神経節細胞密度は野生型マウスとNrf2ノックアウトマウスでは差が認められなかったが、軸索挫滅7日後の網膜神経節細胞密度は野生型とNrf2ノックアウトマウスでは有意な差が認められた。軸索挫滅7日後の網膜神経節細胞密度は対照群に対し、Nrf2活性剤投与群は有意な上昇を認められた |
|
また、軸索挫滅1日後網膜においてNrf2の核内移行が認められ、生体防御酵素「NQO1」、「HO-1」、「GSTA4」、「TXNRD」の発現も有意に上昇し、Nrf2が神経節細胞の保護に関与していることが確認された。さらに、Nrf2活性剤を前投与することで、網膜の生体防御酵素遺伝子「Nqo1」、「Ho-1」、「Gclm」、「Gclc」、「Gsta4」、「Txnrd」の発現上昇に成功し、軸索障害7日後の神経節細胞密度はNrf2活性剤投与群において有意な上昇が認められた(画像4・5)。
以上の結果より、Nrf2は神経節細胞障害時に抗酸化・解毒酵素の発現増加を誘導し、自己防御における神経保護作用に貢献することが明らかになったというわけだ。また今回の成果により、Nrf2活性剤の神経保護作用が明らかにされ、今後、Nrf2は緑内障における新規治療ターゲット分子となる可能性が期待されるとしている。