理化学研究所(理研)は5月15日、科学技術振興機構(JST)、東京医科歯科大学(TMDU)、玉川大学との共同研究により、ラットを用いた電気生理学的解析により、うつ病関連物質(神経伝達物質)の「セロトニン」の活動を制御する脳領域「外側手綱核」が、レム(Rapid Eye Movement:REM)睡眠も制御することを発見したと発表した。
成果は、理研 脳科学総合研究センター 発生遺伝子制御研究チームの岡本仁チームリーダー、同・相澤秀紀客員主管研究員、同・脳回路機能理論研究チーム、同・神経回路・行動生理学研究チーム、JST、TMDU、玉川大の研究者らの共同研究チームによるもの。研究の詳細な内容は、5月15日付けで米国科学雑誌「Journal of Neuroscience」オンライン版に掲載される予定だ。
社会的な問題となっているうつ病にはいくつかの症状があるが、その主な内の1つに不眠症がある。睡眠には、速い眼球運動を伴い、夢を観ていることが多いレム睡眠と、それ以外のノンレム睡眠に分けられるのは、よく知られている。
健常者の場合、入眠後はノンレム睡眠→レム睡眠→ノンレム睡眠という周期を繰り返す。しかしうつ病患者の場合は、レム睡眠が強固に安定化し、入眠後より短時間でレム睡眠が出現したり、レム睡眠中の急速な眼球運動が増加したりする傾向がある。しかし、このような睡眠障害がどのようにして起こるのかは不明なままであった。
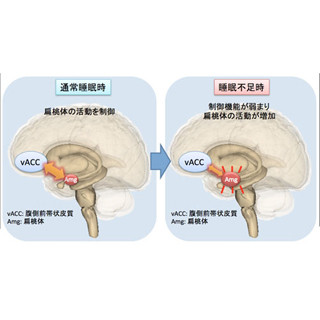
またうつ病の原因となる病巣の候補として、近年、脳の中心部にある外側手綱核が注目されている。この部位は魚からヒトまでが持っている進化的に古い脳の領域だ。外側手綱核を電気刺激により活性化すると、セロトニンを分泌する神経細胞の活動が弱まることから、外側手綱核はセロトニン神経系の制御中枢として知られてきた(画像1)。なお、うつ病はセロトニン枯渇により症状が悪化し、抗うつ薬の多くがセロトニン神経伝達を促進する効果を持っていることから、セロトニンはうつ病の病態に関与すると考えられている。
画像1が、今回の研究の背景となる神経回路を示す模式図。ラット脳の縦断像で外側手綱核によるセロトニン神経活動の制御を示している。脳の中心部に存在する外側手綱核(赤色)は、「抑制性神経細胞」(水色)を介してセロトニン含有神経細胞の豊富な領域(縫線核、青色)へ作用し、セロトニン分泌を抑えるという仕組みだ。セロトニンは、学習・記憶形成に重要な大脳側頭葉の内下部にある「海馬」に作用して、レム睡眠時に発生する特徴的な神経活動を制御すると考えられている(青色矢印)。
前述したように、セロトニンの枯渇がうつ病の症状を悪化させることから、「外側手綱核の過剰な活性化がセロトニン神経系を過度に抑制し、うつ病の症状を悪化させる」という仮説が注目されるようになってきた。実際、fMRI(機能的核磁気共鳴画像装置)などを用いた研究では、うつ病患者の外側手綱核で血流量が異常に増加して、脳の神経活動が活性化している様子がわかってきている。さらに、うつ病に似た症状を示すラットでも、外側手綱核での神経伝達効率が上がっていることが確認済みだ。
しかし、外側手綱核の機能は不明な点が多く、睡眠障害に代表されるうつ病症状と外側手綱核の関係の詳細はよくわかっていないのが現状である。そこで研究チームは、ラットの外側手綱核と睡眠中に顕著となる脳のリズム活動の関係解明に挑んだ次第だ。
研究チームはまず、海馬で起きる振動性の脳神経活動「海馬シータリズム」に着目した。海馬シータリズムは、1秒間に5~8周期繰り返される振動性脳活動だ。レム睡眠中のほかに歩行中や不安・恐怖などの情動行動の際にも観察され、同様のリズムを発生するほかの脳領域との協調活動を通して、これらの行動中の情報処理を担うものと考えられている。
ラットのようなげっ歯類でも海馬シータリズムはレム睡眠や不安などを感じた時だけに発生する特殊なリズム活動だ(画像2)。睡眠中のシータリズムを観察すると、その動物がレム睡眠中なのかノンレム睡眠中なのかを判別することができる。
画像2がレム睡眠と海馬シータリズムで、睡眠中ラットの睡眠ステージと海馬の神経活動の変化を示したものだ。横軸は時間経過(15分間)、縦軸は海馬の神経活動の周波数、色は神経活動における各周波数成分の強度(パワー)で、赤ほど強く、緑ほど弱い活動を示している。前述したように、通常の睡眠ステージは「覚醒→ノンレム睡眠→レム睡眠→覚醒」のサイクルを繰り返す。また、ラットがレム睡眠に入ると、シータリズムの特徴である5~8Hzの神経活動が優位となる。
まず、外側手綱核がレム睡眠の発生と維持に果たす役割を調べるため、外側手綱核を破壊したラットを作製し、レム睡眠の長さが調べられた。その結果、外側手綱核を破壊すると、総睡眠時間に占めるレム睡眠の割合が約41%も減少した(画像3)。また、レム睡眠は睡眠中に何度か繰り返されるが、外側手綱核の破壊は1回あたりのレム睡眠時間を約24%短くする効果があった(画像4)。これらは、外側手綱核がレム睡眠の維持に重要な役割を果たしていることを示しているという。

|

|
|
外側手綱核のレム睡眠持続における役割。外側手綱核の睡眠制御における役割を調べるため、対照群(青)と外側手綱核を破壊したラット(赤)の睡眠ステージの変化が調べられた。睡眠全体に占めるレム睡眠の割合(画像3(左))と1回のレム睡眠の長さ(画像4)のいずれにおいても、外側手綱核の破壊によりレム睡眠の持続性が阻害されている |
|
次に、外側手綱核がレム睡眠中にどのように活動するかを調べるため、睡眠中の野生型ラットを用いて外側手綱核と海馬の神経活動を同時に計測した。その結果、ラットがレム睡眠に入り海馬シータリズムが出現すると、外側手綱核の神経細胞が、シータリズムと同期して活動するようになったのである。つまり、外側手綱核は海馬と協調して活動していることが明らかとなったというわけだ。
今回の成果により、セロトニン制御中枢として知られてきた外側手綱核が、睡眠制御という新たな機能を持つことが示された。これは、うつ病関連物質であるセロトニンと睡眠との関係を明らかにする手がかりとなるという。
また研究チームは、外側手綱核の過剰活性化が、うつ病患者に見られるレム睡眠の強固な安定性の原因である可能性が出てきたともコメント。今後、外側手綱核の過剰活性化がレム睡眠に与える影響を調べることにより、うつ病患者における睡眠異常の病態が明らかにされるものと期待できるとしている。