東北大学は5月10日、白血球などにつかまらず、効率よく目標の臓器・器官に届く事が可能な新規医療用ナノ粒子を開発したことを発表した。
同成果は同大 未来科学技術共同センター(NICHe)の阿部敬悦 教授、原子分子材料科学高等研究機構の阿尻雅文 教授、医学系研究科の川上和義 教授、加齢医学研究所の福本学 教授らによるもの。また、日本農芸化学会2013年度大会において、トピックス賞に選出された。
日本の死因第1位である「がん」は、近年の診断・治療技術の進歩により早期に発見される症例が増加し治療成績も向上しつつあるが、薬剤への不応性に起因する再発がんの増加や、早期発見が困難な深部がんの診断・治療が課題として残されている。また、日本の死因2位、3位の心疾患(心筋梗塞)、脳血管疾患(脳梗塞)は原因となる不安定動脈硬化病変を早期に発見することで予防および治療が期待できるものの、その診断法の開発も始まったばかりという状況である。
その一方で、愛玩動物を家族の一員と考える傾向が強くなっており、愛玩動物医療のニーズが高まるとともにその高度化が進んでいる。愛玩動物も高齢化が進んでおり、その疾病構造も人間と類似してきており、がんや動脈硬化を基盤とする生活習慣病の治療・予防が必要になってくると考えられている。
現在、このようなヒトや愛玩動物の医療における重要課題に対処するための有効な診断、治療法や治療薬の開発が進められており、それを支える小動物実験に使用できるイメージング技術の活用が期待されるようになってきているが、MRIやCTによるイメージングでは固体ナノ粒子がイメージング試薬として利用できるものの、静脈内に投与したナノ粒子のほとんどが肝臓や脾臓などの細網内皮系(網内系)に捕捉され(マクロファージの貪食)、標的組織へ送達できないことなどが大きな課題となっていた。
もし、網内系に捕捉されないナノ粒子を創成できれば、少投与量(マイクロドーズ)で高性能な診断・治療用のプローブを達成できることから、その実現が求められてきた。
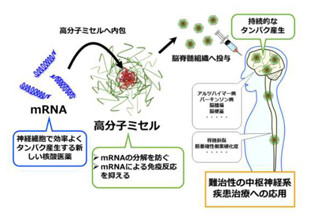
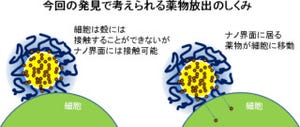
研究グループはこれまで、発酵・醸造に使用される黄麹菌「Aspergillus oryzae」の産生する界面活性タンパク質「hydrophobin(RolA)」に関して、高分子ポリマーの分解促進因子としての研究を行ってきたほか、近年の研究から、ある種の糸状菌のhydrophobinが人の免疫応答回避(ステルス)能を有することを示すことが知られており、今回、これらの背景から、酸化鉄ナノ粒子を、安全な黄麹菌hydrophobin RolAで被覆してステルス能と水溶性を賦与した新規ステルスナノ粒子の開発に挑んだ。
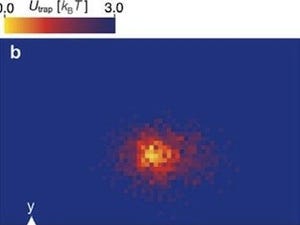
実際に、RolA被覆粒子による動物細胞を用いた免疫応答評価試験の結果、樹状細胞はサイトカイン(免疫反応の結果出てくる細胞間情報伝達性タンパク質)を産生しないこと、ならびにマクロファージによる貪食が回避されることが確認され、ステルス能を持つことが示された。 また、同被覆粒子の各pHでのゼータ電位を測定した結果、中性付近では大きな負電荷を帯びており、血中でも高い分散性(血中で凝集すると免疫系に見付かりやすい)を有することが予想され、in vivoにおける医療用ナノ粒子としての可能性が示されたとする。
なお、研究グループでは、今後、今回開発されたRolA被覆ナノ粒子を用いた、動物試験を通じて、ステルスナノ粒子のマウスなどの動物への個体試験を行い、最終的にはヒトへの応用を目指す計画としている。