京都大学は10月5日、雌のマウスの胚性幹細胞(ES細胞)と人工多能性幹細胞(iPS細胞)から卵子の作製に成功し、なおかつそれらの卵子から子供を産み出すことにも成功したと発表した。
成果は、京大 医学研究科の斎藤通紀教授、同・林克彦准教授らの研究グループによるもの。研究の詳細な内容は、米国東部時間10月4日付けで米国科学誌「Science」のオンライン速報版「Science express」に掲載された。
ES細胞やiPS細胞は、生殖細胞を含む体を構成するいずれの細胞にも分化することのできる細胞である。これらの細胞を任意の細胞に分化させる培養技術の開発は、再生医学領域の前進に貢献するばかりでなく、体内では解析が不十分な発生や生理現象を体外培養により再現できることから、発生・細胞・幹細胞生物学分野においても意義の深いものと考えられている。
卵子や精子を生み出す生殖細胞系列は、生体内の細胞系譜の中で唯一次世代に遺伝情報を伝達できる細胞系列であり、その発生異常は不妊や次世代の個体の疾患に深く関わってしまう。
すべての卵子や精子の起源となる細胞は「始原生殖細胞」と呼ばれ、個体の発生過程の比較的早い段階で分化する。始原生殖細胞はさまざまな発生過程を経て、雌では卵子に、雄では精子に分化するが、その発生過程の多くが胎仔期に行われていることもあり、解明されていない部分が多く残されている。
2011年までに、研究グループは雄のマウスのES細胞やiPS細胞から始原生殖細胞に類似した「始原生殖細胞様細胞(Primordial Germ Cell-like Cells:PGCLCs)」を試験管内で分化させ、それらを基に健常な精子と子孫を得ることに成功している。これにより、体外で作製したPGCLCsは機能的な精子まで分化する能力があることが明らかとなったが、これらが卵子へ分化できる能力を持つかどうかについては不明だった。
そこで研究グループは今回、精子を作製する際に用いたPGCLCsの培養方法を応用して、マウスの雌のES細胞やiPS細胞から卵子を作製する培養技術を開発する研究を進めたのである。
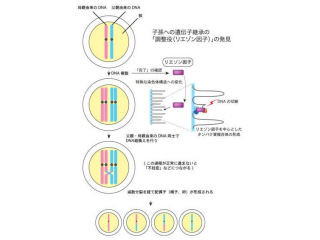
正常な卵子は雌の始原生殖細胞から生じることが知られているために、まず今回の研究では新たに雌のES細胞を樹立した。このES細胞は、始原生殖細胞に発現する遺伝子「Blimp1」と始原生殖細胞や卵子に発現する遺伝子「Stella」が発現している場合に、蛍光タンパク質が発現するように遺伝子(レポーター遺伝子)を改変したマウスから樹立した形だ。
これにより、始原生殖細胞または卵子に分化した細胞は蛍光タンパク質によって光を発するため、蛍光顕微鏡下で容易に観察できる。このレポーター遺伝子を持つ雌のES細胞から、精子が作製された時と同様の方法で、PGCLCsを分化させたのである。
これまでの研究により、ES細胞やiPS細胞から試験管内で分化させたPGCLCsは、培養1週間程度で発生を停止することが明らかになっていた。つまり、このままでは卵子まで分化させることは不可能ということである。
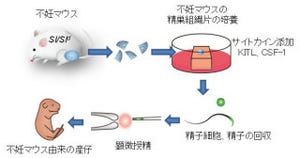
そこで、今回の研究グループはマウス胎仔の中から将来の卵巣になる体細胞の「雌生殖巣体細胞」を取り出し、ES細胞から分化させたPGCLCsと共に培養(凝集培養)を行った(画像1)。これにより、凝集された細胞塊中のES細胞由来のPGCLCsは増殖を開始したのである。
また、生体内の始原生殖細胞の発生過程に起こるX染色体の再活性化や刷り込み遺伝子の消去、減数分裂への移行がES細胞由来のPGCLCsで観察された。これらのことから雌生殖巣体細胞の助けにより、PGCLCsは発生の停止を回避できることが明らかとなったのである。
次に、雌生殖巣体細胞とES細胞由来のPGCLCsの細胞凝集を、免疫拒絶反応を起こさない雌のマウスの卵巣被膜下に移植した。その結果、約4週間後の移植片に未成熟な卵子が多数観察された(画像2~5)。
移植片より採取したこれらの未成熟卵子は、Stellaの発現制御下にある蛍光タンパク質を発現しており、ES細胞から分化させたPGCLCs由来であることが確認された形だ。
|
|
|
|
画像2(左):PGCLCsと雌生殖巣体細胞との凝集塊を移植してから約4週間後の移植片の写真を蛍光顕微鏡写真と合成したもの。移植片の中に蛍光を発する未成熟卵子がいることが観察される。画像3:移植片から採取された未成熟卵子 |
|
|
|
|
|
画像4(左):未成熟卵子の写真を蛍光顕微鏡写真と合成したもの。青色の蛍光タンパク質を発現する様子がわかる。画像5:体外培養により成熟させた受精可能な成熟卵子 |
|
さらに、これらの未成熟卵子を体外培養条件下で卵子を成熟させることにより、受精可能な成熟卵子を得ることに成功。これらの成熟卵子を精子と体外受精させることにより得られた受精卵を仮親の雌マウスに移植した結果、健常なマウスが世界で初めて得られたというわけだ(画像6・7)。このマウスは正常に発達し、雌雄ともに生殖能力があると確認された。
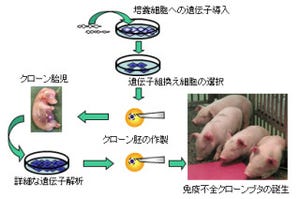
上記の研究に加え、雌の胎仔の「繊維芽細胞」から樹立したiPS細胞から卵子を作製する実験が行われた(画像8・9)。実験に用いたiPS細胞はレポーター遺伝子を持たないことから、始原生殖細胞に発現する表面抗原「SSEA1」と「Integrin-β3」を認識する抗体により、iPS細胞から分化させたPGCLCsが採取された形だ。
|
|
|
|
画像8(左):iPS細胞から分化させたPGCLCsと雌生殖巣体細胞との凝集塊を移植してから約4週間後の移植片から採取された未成熟卵子。画像9(右):体外培養により成熟させた受精可能な成熟卵子 |
|
それらを用いて、ES細胞を用いた場合と同様の凝集培養と雌マウスへの移植が行われた結果、受精可能な成熟卵子の作製、健常マウスの取得に成功した(画像10~12)。
研究グループによれば、今回の成果は基礎および応用面の双方において大きな効果が期待できるとする。基礎面においては、始原生殖細胞の発生メカニズムの解明や卵子形成の初期段階の解析が可能になることだ。
生体内の始原生殖細胞は非常に少数であり、その増殖や分化のメカニズムや、卵子形成の初期段階である減数分裂への移行メカニズムなどに不明な点が数多く残されている。
今回の研究による体外培養技術の開発によって、多数のPGCLCsを容易に作製でき、それらと雌生殖巣体細胞との相互作用を調べることが可能となった。今後はこの体外培養技術を用いて、始原生殖細胞の増殖や分化のメカニズムや、減数分裂への移行メカニズムを明らかにできると考えられるとする。
また応用面においては、不妊症の原因究明に効果が期待できるという。この体外培養技術では、ES/iPS細胞を起点として、始原生殖細胞から卵子形成の初期段階までの一連の分化過程を追えることから、この培養系を発生モデルとして用いて、始原生殖細胞の発生や卵子の分化・成熟に必要な遺伝子の単離に貢献すると考えられる。
また、そうした過程で関連する遺伝子はヒトの不妊症の原因遺伝子となっている可能性もあるという。特に、iPS細胞からも卵子を作製できることから、不妊症患者からのiPS細胞を用いることにより、疾患原因遺伝子の同定を行うことが可能になると考えられるとした。
しかし、今回の研究はマウスを用いた試験段階であり、マウスとヒトの相違点を考慮すると、応用面での貢献のためには、さらなる基礎研究が必要であるという。また、卵子は生命の根源となる細胞なので、倫理的な課題を慎重に検討する必要があると考えられるとも研究グループはコメントしている。