|
九州大学大学院医学研究院臨床検査医学分野の康東天教授、後藤和人助教と、佐々木勝彦氏(民間等共同研究院、LSIメディエンス)らの研究グループは、リボ多糖(LPS)により免疫細胞から産出されるインターロイキン6の量が、ミトコンドリアの特定の機能により調節されていることを明らかにした。さらに、マウスの敗血症モデルを用いて、独自に作成したp32部分欠損マウスにおいて生存率が低下することを見出した。本研究成果は、Cell誌とLancet誌がサポートする新規オープンアクセス誌EBioMedicineに公開された。
敗血症は世界で1,800万人が罹患し、医療の進んだ先進国においても死亡率が30%程度と推定されるため、さらなる治療法の開発が必要とされている。これまでの研究において、敗血症予後は、ミトコンドリアの機能や血中のインターロイキン6の量に相関することが示されていた。
同研究グループは、ミトコンドリア機能を阻害する薬剤をスクリーニングして、ミトコンドリアタンパク質を合成する機能が大腸菌由来のLPSに対するインターロイキン6の算出に影響を与えていることを見出した。また、ミトコンドリアたんぱく質の合成を制御する分子の1つであるp32という遺伝子の部分欠失マウスを樹立し、敗血症モデルではこのp32という遺伝子がインターロイキン6の量と予後に影響を与えていることを見出した。さらに、線維芽細胞やマクロファージなどの細胞を用いて、過剰に産生されるインターロイキン6は、ATF4という分子が核に移行することにより起こるメカニズムであることを明らかにした。
 |
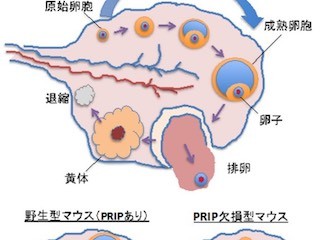
インターロイキン6の過剰産生により、敗血症モデルのマウスの生存率が低下 |
以上の結果を踏まえ、ミトコンドリアの特定の機能を保護することやATF4という分子を阻害することが重症な敗血症の新たな治療のターゲットになると期待される。本研究の研究者は、「世界中の多くの患者が敗血症により命を落としている。研究をさらに前に推し進めて、新たな臨床検査法・創薬の開発などへとつなげて行きたい」と述べている。