理化学研究所(理研)は4月29日、米・Joint Genome Institute、およびデンマーク・コペンハーベン大学との共同研究により、これまで知られていなかった数1000種類のRNAがiPS細胞やES細胞の核内で発現していることを見出し、その一部が幹細胞に特徴的な多能性の維持に関与している可能性があることを明らかにしたと発表した。
成果は、理研 ライフサイエンス技術基盤研究センター 機能性ゲノム解析部門のピエロ・カルニンチ部門長、同・トランスクリプトーム研究チームのアレクサンダー・フォート研究員、同・橋本浩介研究員らの国際共同研究チームによるもの。研究の詳細な内容は、日本時間4月29日付けで米科学誌「Nature Genetics」オンライン版に掲載され、印刷版にも掲載される予定だ。
理研も参加している、米国立衛生研究所(National Institutes of Health:NIH)の国立ヒトゲノム解析研究所(National Human Genome Research Institute)を中心として、2003年9月から正式に開始された国際プロジェクト「ENCODE(Encyclopedia of Human DNA Elements)」は、ポストゲノム戦略として米国で立ち上げられたプロジェクトだ。完全解読されたヒトゲノム上に遺伝子の機能を担う領域をすべて書き込んで全ヒトゲノム(DNA)の百科事典を作成することを目指しており、これまでに転写産物(RNA)の網羅的な解析を行い、ヒトゲノムの70%以上が転写されている事実を明らかにした。
また、理研が主宰する世界20カ国114の研究チームが参加する国際研究コンソーシアム「FANTOM(Functional ANnoTation Of Mammalian cDNA)」は、ほ乳類の「トランスクリプトーム(細胞内の全転写産物=全RNA)」解析を行い、タンパク質をコードしない「ノンコードRNA(ncRNA)」には「レトロトランスポゾン」に由来する配列が多く含まれていることを明らかにしてきた。
レトロトランスポゾンとは、HIVなどのレトロウイルスのように、DNA→RNAへの転写と、RNA→DNAへの逆転写によって増殖する性質を持つ遺伝因子のことで、ゲノム上のレトロトランスポゾンが転写されてRNAになり、さらに逆転写酵素によりDNAに戻ることでゲノム中を移動しコピー数を増やすという仕組みを持つ。このような配列は、HIVのようなレトロウイルスがゲノムに組み込まれた後の残骸であると考えられており、ヒトゲノムの進化の過程で、ほとんどのレトロトランスポゾンは不活性化されたとされているが、その生物学的な機能はわかっていなかった。
ES/iPS細胞は、創薬、再生医療への応用が進められており、これらの幹細胞の性質を深く理解することがより重要な課題となっている。幹細胞に特有の転写制御ネットワークについての先行研究には、ncRNAの役割の解明も含まれてはいるが、既知のncRNAだけを機能解析の対象としていたため、限られた知見しか得られていないという課題があった。
そこで研究チームは今回、理研が独自開発した「CAGE(Cap Analysis of Gene Expression)」法を始めとする複数のRNA解析技術に加え、細胞質に比べて分子数の少ない核内のRNAを濃縮して抽出することで、ほ乳類の幹細胞に存在する全RNAの完全な解析を試みたのである。
なおCAGE法とは、耐熱性逆転写酵素やcap捕捉法を組み合わせて転写物の5'末端の塩基配列を決定する実験手法のことだ。この塩基配列を読み取ってゲノム配列と照らし合わせて、どこから転写が始まっているかを調べることができ、遺伝子の転写開始点をゲノムワイドに同定することも可能である。
ちなみに今回の実験で多能性幹細胞のサンプルとして用いられたのは、ヒトおよびマウスから作られたES細胞(ヒト3種、マウス3種)とiPS細胞(ヒト2種、マウス3種)の計11種。また分化した細胞のサンプルとして、iPS細胞の樹立に用いられた6種の細胞が対照に用いられた。
それぞれの細胞について、核内RNAと細胞質RNAを別々に調製し、CAGE法や「RNA-seq(RNA sequencing)」法など複数の手法を用いてトランスクリプトーム解析が行われた。RNA-seq法は、組織や細胞で発現している全RNAを解析する手法である。メッセンジャーRNA(mRNA)やncRNAの断片的な配列情報(数10~数100塩基)を網羅的に取得し、ゲノム配列と対応させることで、遺伝子発現量の定量や新たな転写配列の発見を行うというものだ。
その結果、これまで知られていなかった幹細胞特異的な転写産物「NASTs(Non-Annotated-Stem-Transcripts)」が核内で多量に発現していることが見出されたのである。NASTsはヒトで3042種、マウスで8873種も発見され、両者で共通する配列は少ないものの、どちらも約3分の1はレトロトランスポゾンに由来する配列が含まれていたという。
特に、レトロウイルスに特徴的なウイルスゲノムの両端に位置する繰り返し配列であり、宿主ゲノムに挿入されると強い転写活性を発揮し、ウイルスゲノムの発現を促進する機能を持つ「長鎖末端反復配列(Long Terminal Repeat:LTR)」から転写されるNASTsが多く、これらのLTRは、DNAの相互作用や「エンハンサ」(遺伝子の上流や下流に位置し、遺伝子の転写効率を変化させるDNAの特定の配列の内、転写効率を著しく高める領域(配列))の活性の推定から、幹細胞においてクロマチン構造や細胞周期に関わる遺伝子の発現制御に関わっている可能性が示唆されたとする。
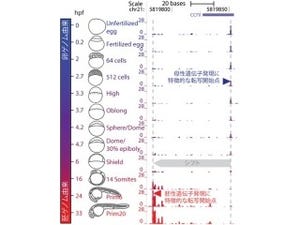
画像1はNASTsに存在する繰り返し配列のグラフだ。CAGE法で決定されたRNA配列を既知のレトロトランスポゾンと比較された上で分類されている。「MaLR」、「ERVL」、「ERVK」、「ERV1」はLTR型のレトロトランスポゾンであり、マウスおよびヒトで頻繁に見つかった。
さらに、LTR由来のNASTsが幹細胞の多能性維持に果たす役割を調べるため、「si(small interference:短い2本鎖)RNA」法によるNASTの機能阻害実験を行い、Nanogなどの多能性マーカー遺伝子の発現が変化するかが調べられた。siRNA法は、短い2本鎖RNAを細胞に導入し、任意の遺伝子の阻害をする実験手法のことである。2本鎖RNAによって配列特異的にRNAが分解されるRNA 干渉(RNAi、RNA interference)の原理に基づいたものだ。
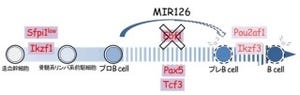
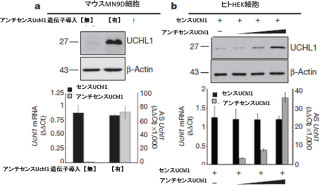
マウスのiPS細胞で特に強く発現している77種のNASTsについてそれぞれ機能阻害実験が行われたところ、4種のNASTsの機能阻害で、Nanog遺伝子、Sox2遺伝子、Oct4遺伝子などの多能性マーカー遺伝子の発現が低下することが確認された(画像2)。この結果は、LTR由来のNASTsが、多能性維持に必須な転写制御ネットワークに直接関与していることを示唆するという。
これまで、ヒトゲノムに存在するレトロトランスポゾン由来の配列は、ヒト進化の過程でレトロウイルスがゲノムに挿入した残骸であり、機能を持たない「ジャンクDNA」と考えられてきた。LTRに由来するRNAが幹細胞特異的に発現し、幹細胞の性質や多能性の維持に関与していることを示唆する今回の成果は、幹細胞生物学におけるncRNAの重要性を示すものだという。
画像3が、ほ乳類ゲノムにおけるNASTsの起源と幹細胞における機能の推定だ。ほ乳類の進化において、レトロウイルスの感染とレトロトランスポゾンの活発な転移がしばしば生じたと考えられている。現存生物には、その残骸がゲノムの広範囲にわたって存在しており、その一部はタンパク質をコードしないncRNAとして発現しているという具合だ。その中でもNASTsは、幹細胞の性質の制御に関わっている可能性があるというのが、今回の成果である。
今後さらにNASTsの機能を解明することで、幹細胞の理解、多能性を制御する転写制御ネットワークの解明が進み、iPS細胞などの幹細胞から目的の細胞を効率よく分化させる方法の開発などへの応用が期待できるとした。