富士フイルムは6月11日、再生医療に必要な細胞生育・増殖のための「足場」(=細胞外マトリックス)として再生医療用に新開発したヒトコラーゲン型タンパク質「リコンビナントペプチド(RCP)」を用いて厚さ1mmを超える細胞集合体を作り、その細胞集合体を移植して、生体組織と結合した血管を細胞集合体に形成させることに成功したと発表した。
今回の実験では、移植後すみやかに細胞集合体と生体組織との間に血管形成が認められ、移植後4週間以上にわたって移植細胞が生存していることが確認されたことも、併せて発表されている。
なお、今回の研究成果は6月12日~14日にパシフィコ横浜において開催される「第11回 日本再生医療学会」の口頭発表およびランチョンセミナーで、発表される予定だ。
再生医療は、人工的に培養した細胞や組織などを移植して、損傷した臓器や組織を再生し、患部の機能を回復させる医療技術である。他人からの臓器移植や、人工臓器による治療に替わるものとして期待されると同時に、現在、治療法がない難治性疾患に対する新たな治療法として注目されている状況だ。
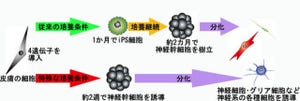
これまでに、多様な体性幹細胞の培養法が確立され、またiPS細胞の研究進展によりさまざまな細胞の再生医療への使用が現実的になってきた。
しかし、一方では、培養した細胞の生体への移植方法は未だに開発途上にある。例えば、厚さ400μmを超える細胞集合体は、移植後に栄養や酸素の供給を内部まで十分に行うことができないため、体内に移植することは困難といわれてきた。
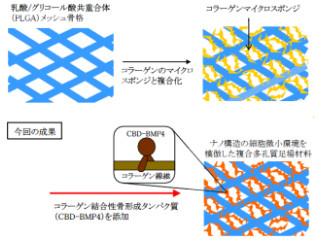
今回、富士フイルムは、細胞が正常に生育・増殖するために必要な足場として、RCPを用いて体外で厚さ1mmを越える細胞集合体を作ることに成功した次第だ。なおRCPは、ヒトコラーゲンの遺伝子を酵母細胞に組み込み、遺伝子工学により細胞培養によって新たに作製された。
また、ジャパン・ティッシュ・エンジニアリングと共同で、これを動物に移植して、集合体内部の組織が2週間以上にわたって生存したことを確認。
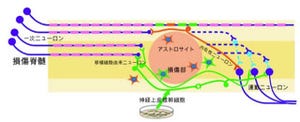
さらに、細胞集合体に血管内皮前駆細胞を組み込むことで、移植した細胞集合体内に5日間で血管を形成させ、細胞集合体と生体組織との間で血管を結合させることに成功したのである。これにより、移植後4週間以上の生存が確認でき、細胞の持続的な機能発現が可能になったというわけだ。
RCPは、いろいろな臓器の細胞の生存・機能発現に最適なアミノ酸配列を設計できることから、今後、幅広い応用が期待できるという。また、RCPは動物由来物質を用いる必要がないので、狂牛病の原因となるプリオンなどの動物由来の病原体を一切含んでいない。
生体内で分解された場合にも、周辺の組織を傷める酸などの生成がないことなどから、再生医療の足場材及び培養基材として有用であると考えられている。
富士フイルムは、これらの結果は「大きな再生医療用の組織を移植して、患者の体内で機能させること」を可能にするもので、今後、再生医療の発展に大きく貢献できる画期的な研究成果とした。
また、今後はこれまで培ってきた技術・ノウハウを生かして、再生医療分野の研究開発をさらに推進し、再生医療の発展に貢献していくとしている。