横浜市立大学は、発育不全、重度の精神遅滞、小頭、まばらな頭髪およびまつ毛、特異な顔貌、手足の第5指のツメの無形成を特徴とする先天的異常症候群「コフィン-シリス症候群(Coffin-Siris Syndrome:CSS)」の原因となる遺伝子(責任遺伝子)を解明したと発表した。
成果は、横浜市立大学学術院医学群の鶴崎美徳助教、同三宅紀子准教授、同松本直通教授(遺伝学教室)らの研究グループと、大阪府立母子保健総合医療センター、埼玉県立小児医療センター、信州大学医学部、日本赤十字社医療センター、琉球大学医学部、お茶の水女子大学、山形県日本海総合病院、山形大学医学部、広島市こども療育センター、自治医科大学医学部、南カリフォルニア大学医学部、愛知県心身障害者コロニー中央病院、中川の郷療育センター、獨協医科大学越谷病院、横浜市立大学医学部(生化学教室)、北海道医療大学との共同研究によるもの。詳細な研究内容は、英科学誌『Nature Genetics』オンライン版に日本時間3月19日付けで掲載された。
CSSは1970年にCoffin博士とSiris博士によって報告され、冒頭で述べたような特徴を有する先天的異常症候群だ。手足の第5指の末節骨とツメが無形成であることが多いため(図1)、第5指症候群とも呼ばれている。責任遺伝子は、これまで明らかになっていなかった。
松本教授らのグループは、集積したCSSの23症例の内、臨床症状から典型例5例を対象に「全エキソーム配列解析」を実施した。全エキソーム配列解析とは、遺伝子のエクソン部分(実際に利用される部分)を全ゲノムにわたって網羅的に分画した後、次世代シーケンサを用いて塩基配列を決定する方法のことだ。
そして5症例中2症例で、「SMARCB1」遺伝子に「新生突然変異」(両親から引き継がれた変異でなく、その個体において突然発生した変異)が見出された。
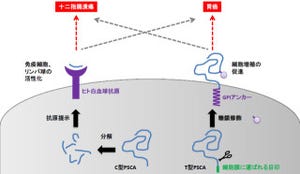
同遺伝子は、クロマチン再構成因子の1種である「SWI/SNF複合体」のBAF型の構成成分であることから、さらに残りの21症例を対象に、SWI/SNF複合体の各構成サブユニットをコードする15遺伝子に対して変異解析を行い、21症例中18症例でSMARCB1と一緒に働くタンパク質の遺伝子群、「SMARCA4」、「SMARCE1」、「ARID1A」、「ARID1B」、あるいは「SMARCA2」のいずれかに変異が認められたという具合だ(画像2)。
これまでSWI/SNF複合体因子の異常はさまざまな腫瘍の「体細胞変異」(生殖細胞ではない一般的な細胞に生じる変異で、子孫に変異は伝わらない)として、あるいは「神経鞘腫症」や「ラブドイド様腫瘍易罹患症候群」の「生殖細胞系列変異」(生殖細胞の精子または卵子に生じる変異で、子孫のすべての細胞のDNAに組み込まれる)として報告があった。
今回の松本教授らのグループの研究で、SWI/SNF複合体の異常が腫瘍関連疾患のみならず精神発達遅滞/先天奇形症候群を惹起することが証明され、SWI/SNF複合体の新たな機能的側面が明らかとなった次第だ。
これまでCSSの診断は臨床症状のみで行われ、症例ごとの差異などから診断は容易ではないという面があった。ただし、CSSの大部分(87%)が今回同定された責任遺伝子群の異常で説明可能となり、CSSの確実な遺伝子診断法が実現した形だ。責任遺伝子が解明されたことで、CSSの病態解明と治療法の開発や病態改善などが大きく進展すると期待されると、研究グループはコメントしている。