科学技術振興機構(JST)、京都大学、学習院大学の3者は1月26日、認知症や心機能の抑制に関係するヒトの「ムスカリン受容体」の立体構造をX線結晶構造解析によって解明したと共同で発表した。研究は京都大学大学院医学研究科の小林拓也講師、学習院大学の芳賀達也前教授、米スタンフォード大学ブライアン・コビルカ教授らの研究グループによるもので、成果は英科学雑誌「Nature」オンライン速報版に英国時間1月25日に掲載された。
「アセチルコリン」は、世界で最初に神経伝達物質の1つであることが証明された物質だ。アセチルコリンには、ニコチン作用とムスカリン作用が存在することが古くから知られており、各々に特異的なアセチルコリン受容体(ニコチン受容体とムスカリン受容体)が同定されている。
副交感神経や運動神経の末端から分泌されたアセチルコリンは、骨格筋、内臓平滑筋などに存在するアセチルコリン受容体に働き、筋収縮を促進するほか、副交感神経を刺激し、心拍数の減少、脈拍数の減少、唾液の分泌を促進する。このようにアセチルコリンは、基本的な生命現象に深く関与している物質だ。
アセチルコリンは特に脳内においてそのバランスが崩れると、さまざまな疾患が生じてしまう。例えば、アセチルコリンが減少すると自律神経失調症やアルツハイマー病につながるといわれている。またパーキンソン病の患者では、逆にアセチルコリンの相対的な増加が認められているという具合だ。アセチルコリンがムスカリン受容体に結合するのをブロックすることで、パーキンソン病の症状を緩和することが知られており、古くから治療薬として使われている。一方で、副作用として統合失調症や認知症の症状を悪化させることも知られており、一長一短があるというわけだ。
ムスカリン受容体には、M1からM5まで5種類のサブタイプが存在している。例えば、M1受容体は大脳皮質や海馬に多く存在し、記憶や学習に関与しているという。また、M2受容体は主に心臓に分布し、心臓機能を抑制的に調節している。このように各々のサブタイプは固有の分布と薬理作用を持っており、構造に指南されたサブタイプ選択的な創薬が期待されているのが現状だ。
しかし、膜タンパク質であるムスカリン受容体は、可溶性の細胞内のタンパク質と異なり、立体構造を明らかにするために必要なタンパク質の精製や結晶化が困難なため、これまで立体構造が解明されていなかった。そこで、研究グループでは、より効果的で副作用の少ない薬剤の探索・設計に有効なムスカリン受容体の構造情報を得るために、受容体の発現・精製から結晶解析までのさまざまな技術開発と立体構造の解明を試みたのである。
今回の研究では、まずヒトのムスカリンM2受容体遺伝子を合成し、昆虫細胞を用いることで、安定な受容体を大量に発現することに成功。また、「リガンドアフィニティーカラム」(特定の分子と親和性のあるタンパク質のみを固定して精製する方法)を用いて、「リガンド結合活性」(特定の受容体に結合する基質がリガンドの分子が、受容体に結合する働きのこと)のある受容体だけを単一に精製することで、ムスカリンM2受容体の結晶化が可能となった。
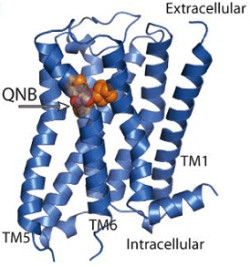
ムスカリンM2受容体は、膜タンパク質の結晶化で効果を上げている「脂質立方相法」(モノオレインなどの脂質からなる脂質二重層内にタンパク質を存在させ、生体膜に近い環境で結晶化を行う方法)を用いて結晶化を行い、X線結晶構造解析によってアセチルコリンがアセチルコリン受容体に結合することを阻害する「抗コリン薬」の1つである「3-キヌクリジニルベンジラート(3-quinuclidinyl benzilate:QNB)」とムスカリンM2受容体の複合体の立体構造を解明した(画像1・2)。
ムスカリンM2受容体の全体構造は、これまでに構造が決定されているGPCRと同様に7本の膜を貫通したらせん構造を持っていることを確認。QNBは、ムスカリン受容体の5種類すべてのサブタイプに共通して存在するアミノ酸に囲まれていた(画像3・4)。また、受容体に結合したQNBに3つの大きなアミノ酸(チロシン残基)がフタのように覆いかぶさっていることから、一度受容体に結合したQNBが受容体から離れにくくなっていることも判明した(画像5)。

|

|
|
画像3。QNBの構造式 |
画像4。リガンド結合部位の様子。QNB(オレンジ色)と周囲のアミノ酸(青色)の相互作用。周囲のアミノ酸のほとんどのものが、M2以外のムスカリン受容体サブタイプでも保存されている |

|
|
画像5。結合しているQNBにフタのように覆いかぶさっているチロシン残基(Y403、Y426、Y430)。トリプトファン残基(W422、黄色)はアロステリックリガンドの結合に関与していることが示唆されているアミノ酸 |
QNBは、アセチルコリンが結合する「オルソステリック部位」(受容体の基質(内在性リガンド)が結合する場所)に結合していることが示されたが、「アロステリック部位」(受容体の基質(内在性リガンド)が結合する場所とは異なる場所で、そこに結合する物質によって受容体機能が影響を受ける場所)はその上部に比較的広い空間として細胞の外側に広がっていることが確かめられたのである(画像6)。
アロステリック部位を構成するいくつかのアミノ酸は、アミノ酸変異実験によりアロステリック部位に結合するリガンドの親和性が低下することが報告されているアミノ酸残基と一致していた。アロステリック部位は、各受容体サブタイプにおいて特徴的なアミノ酸残基が存在している部位だ。従って、各サブタイプに特徴的なアミノ酸残基の側鎖と化合物の官能基の間に相互作用(水素結合など)を生み出すことができ、サブタイプ選択的な化合物の開発につながると考えられている。
創薬分野では近年、タンパク質の立体構造をもとにした創薬戦略(Structure-Based Drug Design)が進行中だ。特に、ヒトが持つ受容体は創薬のターゲットとして注目されており、これらの受容体の立体構造を明らかにすることで、より効果的な薬剤の設計が可能になると期待されている。
今回の研究からムスカリンM2受容体の立体構造が明らかとなり、抗コリン薬の結合部位の詳細情報を得ることが実現したこととなった。研究グループでは、これらの立体構造の情報をもとに、今後はより効果的で副作用のない各受容体サブタイプ選択的な薬の探索・設計が可能になると考えられることことから、パーキンソン病、アルツハイマー病、統合失調症などの治療薬への貢献が期待できるとしている。