自然科学研究機構 分子科学研究所(IMS)理論・計算分子科学研究領域の平田文男 教授の研究グループは、統計力学理論に基づく知的創薬に関する研究に向けた発表を行った。
風邪の症状を抑える薬にはさまざまな化合物、例えばアセチルサリチル酸(アスピリン)、塩化リゾチーム、フマル酸クレマスチンなどが含まれており、それぞれが発熱、のどの痛み、鼻づまりに効く成分と言われている。しかし、ヒトの大きさは1023個以上の分子でできているのに比べ、こうした各種成分はほんのわずかな分子でしか構成されていない。そのため、このような薬が体の中でどのように作用しているのか、数十年前までは全く分からず、近年の医学、薬学、生化学などの発展により、薬の分子がどのようにして病気の原因となるバクテリアやウイルスを退治しているのかが、明らかになってきた。
知的創薬では、まず、生体機能と分子認識が行われる。生物の細胞内では生命を維持したり、子孫に継承したりするためにさまざまな生体分子(タンパク質やDNAなど)が活躍している。例えば、赤血球の中にあるヘモグロビンというタンパク質は肺の中で酸素分子を結合し、それを末端の組織に運ぶ「運送屋」の役割を果たしており、もし、何らかの障害でヘモグロビンが働かなくなると人間は死んでしまう。一酸化中毒では、人間が一酸化炭素を吸収するとヘモグロビンがそれを優先的に結合してしまい、酸素を結合できなくなってしまうために発生する。また、たんぱく分子は糖や脂肪やアルコールなどを分解したり(酵素)、細胞内外の水分を調節したり(水チャネル)などの役割も果たしているが、生物が生命を維持し継承するために生体分子が果たすこうした役割は生体分子の「機能」と呼ばれ、生体分子がその機能を営むためには、その対象となる分子(「リガンド」や「基質」)を自分自身のある特定の場所(活性部位、反応ポケット)に選択的に結合する必要がある(ヘモグロビンの例では、「へム」と呼ばれる場所が活性部位にあたり、酸素分子がリガンドにあたる)。
このような生体分子があるリガンドを選択的に結合する過程をより一般的は「分子認識」と呼ばれ、これは生命現象の最も本質的な素過程と言いかえることができ、もし、この分子認識過程が何らかの原因で阻害されると人間は病気になったり、ひどい場合は死んでしまうことになる。
次に薬がどのように効くかだが、バクテリアやウイルスも生物の一種のため、生きていくために、多くのタンパク質やDNAが機能を果たしており、その素過程として、常に、タンパク質やDNAの分子認識過程が働いている。そのため、もし、バクテリアやウイルスの生存や増殖に不可欠なタンパク質やDNAの分子認識過程を阻害することができれば、これらを死滅させ、病気を治すことができることから、病気を治すために使う薬剤分子の多くが、こうしたバクテリアやウイルスのタンパク質やDNAに優先的に結合して、その機能を阻害する役割を果たすものとなっている。
そして、その薬剤分子がバクテリアやウイルスのタンパク質やDNAに優先的に結合する際の優先順位を決める因子は、熱力学の言葉で「自由エネルギー」と呼ばれ、リガンドや薬剤分子の場合、タンパク質内の活性部位に結合している場合の自由エネルギーの方がタンパク質外(バルク)環境に居る状態より低ければ、それらの分子はタンパク質に「結合」、あるいは「認識」され、その差が大きいほど、より優先的に認識されることになる。そのため、分子認識によって自由エネルギーができるだけ低くなる化合物(分子)を探索することが、創薬の重要なステップの1つとなっている。
この結合の自由エネルギーの決定因子は、タンパク質の活性部位の幾何形状と薬剤分子のそれとの相性(鍵と鍵穴)や、活性部位内の電荷分布と薬剤分子のそれとの相性があるが、この2つだけでは結合の自由エネルギーは決定されない。さらに大きな要因はタンパク質やDNAが存在する環境、例えばタンパク質は水溶液中にあるため、多くの場合その活性部位にも水分子が結合しており、リガンドや薬剤分子が活性部位に結合するためには、その水分子の全部または一部が排除される必要がある。一方、薬剤分子の方もタンパク質に結合する前は水溶液の環境に居るため、その周りには水分子の「衣」をまとっており(水和)、薬剤分子がタンパク質と結合するためには、その水分子の全部または一部を取り除く(脱水和)必要がある、
しかし、従来、「知的創薬」と称して企業や大学で行なわれてきた方法の大部分はこの水和や脱水和の自由エネルギーを無視してきたこともあり、今回、同研究グループがこうした問題の克服に向け、水和や脱水和の自由エネルギーも含めた知的創薬の新しい方法の提案を行った。
具体的には同研究グループでは、これまで液体の統計力学理論の1つである3D-RISM理論を開発し、それを用いて、分子認識過程を含む生体分子機能に関する研究を行ってきたが、今回は、この3D-RISM理論に基づいて、創薬への応用を直接目指した「タンパク質の分子認識過程の研究」を進めてきた。対象としたのは、ホスホリパーゼA2(Phospholipase A2)と呼ばれるタンパク質で、同タンパク質は、発熱や痛みのもとになるアラキドン酸を合成することで知られているほか、近年、非ステロイド性の薬として有名なアセチルサリチル酸(アスピリン)も結合することが実験によって明らかにされるなど、新たな薬の開発にもつながるため、創薬分野でモデルタンパク質の1つとなっている。

|
|
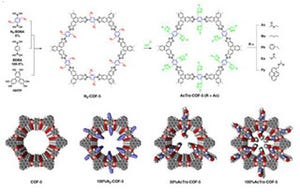
X線構造解析によってとられた、ホスホリパーゼA2にアセチルサリチル酸(アスピリン)が結合する様子。結合ポケットは、カルシウムイオンCa2+(図中、緑色の球)とアスパラギン酸(ASP49)などによって形成されると考えられている |
3D-RISM理論を用いてこうしたタンパク質-リガンド分子系を解くと、タンパク質の内外におけるリガンド分子の分布関数を求めることができる。

|
|
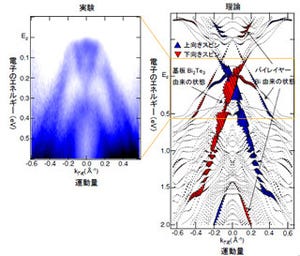
ホスホリパーゼA2に対する3D-RISM理論を用いて計算したアセチルサリチル酸の分布(赤色で表示)。X線構造においてアセチルサリチル酸が存在していた箇所(図中、網目で表示されている箇所)にも分布していることが分かる |
分布関数は、その位置にどのくらいの確率でリガンド分子が存在するかの指標を表す関数(同関数の逆数の対数をとると、水和の自由エネルギーに対応する)で、分布関数が大きい値を取る箇所は、その場所にリガンドが結合しやすいことを意味することから、この分布関数を解析することで、自動的にリガンド分子がどこにどのように結合するのかを知ることができる。
今回の研究では、そうした解析のためのスコア関数を定義し、それに基づいてリガンド分子であるアスピリンの位置および配向の特定を行った。解析結果を調べたところ、3D-RISM理論から予測した構造が実験で得られた構造とほぼ一致していることが判明したという。
これまでもスコア関数を用いた解析は、一般的な創薬研究において行われてきたが、その多くは物理化学的な根拠を持っていなかった。これは鍵と鍵穴のように幾何学的な議論しかしていないことを示すが、今回の研究では、分布関数という物理化学的に重要な意味を持つ量を基にして行われており、研究グループでは、今回のような解析が確立すれば、より確かな創薬研究が可能になると考えられるとしている。