東京医科歯科大学は9月12日、骨を破壊する「破骨細胞」を育てることで骨を作り替える「指令細胞」を発見したと発表した。
同大学大学院医歯学総合研究科 分子情報伝達学分野の高柳広教授と中島友紀助教のグループと、オーストリアIMBA研究所、スペイン国際癌センター、英国Cambridge大学、米国Baylor大学、米国Missouri-Kansas City大学、九州大学大学院工学研究院、東京大学先端科学技術センターによる共同研究によるもので、成果は国際科学誌「Nature Medicine」に、9月12日付けでオンライン版に掲載される。
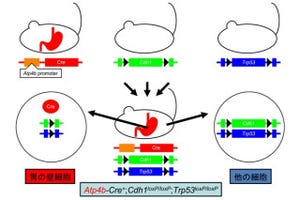
「骨細胞」は、骨を構成する細胞の約90%を占め、骨に埋め込まれた状態で存在する細胞だ。神経細胞様の突起により網目状のネットワークを形成することで、骨内の骨細胞同士だけでなく、骨表面に存在する破骨細胞や、骨形成の役目を担う「骨芽細胞」とも密接に連携している(画像1・A)。
このような特殊な環境状態にあることから、骨細胞は重力による負荷など外界からのメカニカルストレスの感受や細胞間シグナルへの応答に関わり、「骨リモデリング」(骨の破壊と再生の仕組みのこと)を制御する指令細胞の可能性が想定されていた(画像2)。

|
|
画像2。骨リモデリングの図式。破骨細胞による骨の破壊と骨芽細胞による骨の申請が、絶妙なバランスにより保たれ、骨は常に新しく生まれ変わっている。骨リモデリングサイクルにおいて、本文で後述する破骨細胞分化因子「RANKL」を発現する骨細胞が破骨細胞を育て、骨を新しく作り替える指令細胞であることが今回の実験で明らかになった |
しかし、骨という特殊な硬い組織に埋め込まれた骨細胞の単離は難しく、その機能は十分解明されていない状態で、同細胞を巡る研究は激しい国際競争を繰り広げているのが現状だ。
今回の研究では、骨の中に埋め込まれた骨細胞だけを特異的に蛍光発色させる遺伝子「EGFP」を導入した可変マウスを作り出し、酵素処理と「フローサイトメトリー」による細胞分離法を用いて、高純度の骨細胞を単離培養することに成功したという次第である(画像1・B)。
単離された骨細胞は、従来の組織学的検討から判明している「Sost」や「Dmp1」といった遺伝子を特異的に発現しており、骨芽細胞に特異的に発現する遺伝子「Keratocan」などを検出していないという特徴がある。
また、破骨細胞を育てるためには破骨細胞分化因子「RANKL」が必須だ。しかし、骨組織内でどのような細胞がRANKLを発現して破骨細胞を育て、骨を新しく作り替える指令を出しているかは、これまで不明だったのである。
そこで研究チームは詳細な検討を行い、骨や骨髄に含まれる細胞集団の中で、骨細胞が最もRANKLを発現し、破骨細胞を育てる能力に優れていることを見出したというわけだ(画像3A、B)。
さらに、骨細胞だけでRANKL遺伝子が破壊されるマウスも作製。すると、重篤な大理石骨病を発症することが確認された(画像2・C)。この大理石骨病は、生後すぐには発症せず、成長に伴ってその病状が悪化するという特徴がある。これは、成長に伴って外界から受けるメカニカルストレスを骨細胞が感受し、RANKLを発現することが原因であると考えられた。
現在、骨細胞はさまざまな骨疾患の標的細胞として注目を集めている。今回の研究によって開発された骨細胞の単離培養法は、細胞生物学的にいまだ不明な点が多い骨細胞の特製を理解する上での重要なデバイスとして、今後さらなる骨制御因子の同定や新たな治療法の確立につながる可能性を秘めているとした。