キヤノンITソリューションズ(キヤノンITS)は6月18日、製薬企業のMR(医薬情報担当者)および安全管理部門向けに、安全性情報の進捗管理システム「PVLink Report Manager(ピーブイリンクレポートマネージャー)」の提供を開始した。
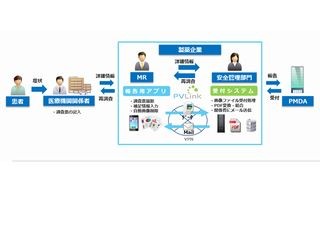
国内の製薬企業は、医薬品の副作用と疑われる症例などを確認した場合、医薬品医療機器総合機構(PMDA)に対する報告が義務づけられており、一般的に副作用情報は製薬企業のMRが医療機関などを訪問して収集し、自社にある医薬品の安全管理部門に報告する。安全管理部門は、報告された情報の評価や調査を実施しPMDAに副作用情報の報告を行う。
この際、安全管理部門は副作用情報の詳細を調査するためにMRと複数回やり取りを行うが、企業によってはMRが数千人にもおよぶため進捗管理の負荷が高く、報告遅延や報告漏れのリスクが運用上の課題となっていることに加え、MRからは外出先からでも社内ルールに沿って安全かつ迅速に報告したいという要望があるという。
同社では、個別症例安全性報告を電子的に伝送するEDIシステム「EDI-Master DEX for Medical」を提供し、2017年に安全性業務効率化を図るPVLinkシリーズ製品のスマートデバイスを利用したMR向け副作用報告システム「PVLink Camera Report」を提供している。
今回、製薬企業からの要望を集約し運用面で課題となっていた安全性情報の進捗管理業務について、基本機能をパッケージ化したPVLink Report Managerを開発。
新製品は、製薬企業における安全性情報を管理する業務プロセス(報告・収集・進捗管理・調査・ICSR連携)の機能を標準装備しており、個別にシステム開発を行った場合に比べて、低コスト、短期間でシステムを構築することができるほか、画面構成・入力項目・デザインなどはユーザーの要望に合わせて設定することを可能としている。
機能の一例として営業部門は、Webによる連絡票の起票および一覧参照、調査期日超過をはじめ条件設定によるアラート表示、管轄担当症例の一覧表示など、安全管理部門では受付情報の統合管理(検索/一覧の参照/編集/登録)、メール送信(受領報告、調査依頼、調査完了メールなど)、症例単位のICSR出力連携を行える。
主な特徴として「進捗管理の見える化」「情報収集から管理、報告まで情報連携を網羅」の2点を挙げている。進捗管理を見える化については、副作用報告の進捗管理がシステム化され、MRからの報告への受領メールも自動化される。
また、MRがスマートデバイスから安全管理部門への報告に使用するPVLink Camera Reportと連携して使用することができる。MRは営業所に戻らずに外出先からスマートデバイスやPCを利用して第一報を報告することができ、報告遅延や報告漏れの防止につながるとしている。
情報連携を網羅することに関してはPVLink Camera Reportと新製品により、副作用情報の収集・進捗管理を行い、個別症例安全性報告を電子的に伝送するEDIシステム「EDI-Master DEX for Medical」を使用してPMDAへの報告を行うことで、安全性情報の統合管理を実現することが可能だという。
同社は、今後も製薬企業の安全性情報管理業務についてトータルなソリューションを展開し「EDI-Masterシリーズ」を中核とするEDIソリューション関連事業で、2022年に年間売上高25億円を目指す。