理化学研究所(理研)は9月16日、iPS細胞から網膜色素上皮細胞(RPE細胞)を分化・誘導し、それらを用いてサルとヒトの免疫拒絶反応モデルを開発したと発表した。
同成果は、理研 多細胞システム形成研究センター網膜再生医療研究開発プロジェクト 杉田直 副プロジェクトリーダーらの研究グループによるもので、9月15日付の米国科学誌「Stem Cell Reports」オンライン版に掲載された。
同プロジェクトでは、2014年にヒトiPS細胞由来RPE細胞をシート状にし、滲出型加齢性黄斑変性患者に世界で初めて移植した。これは自分の細胞を他の場所に移し変える自家移植によって行われたもの。自家移植は、術後に拒絶反応が起こる確率が極めて低いという特徴がある一方で、細胞培養のために膨大な時間と費用がかかるため、同プロジェクトは、次の臨床試験で経費削減とより効率的に細胞の準備ができる他家移植の実現を目指している。
他家移植には京都大学iPS研究所の再生医療用iPS細胞ストックに保存されているヒト白血球抗原(HLA)がホモ接合体のドナーから樹立したiPS細胞を使用する予定となっている。これらの細胞を利用すると、原理的には術後の拒絶反応が抑えられると考えられるが、眼科領域で実際に検証した報告はこれまでになかった。
今回、同研究グループは、移植時の拒絶反応の要因となる主要組織適合抗原(MHC、ヒトではHLA)がホモ接合体のカニクイザルからiPS細胞を樹立。そして、そのiPS細胞から分化・誘導したRPE細胞を他のカニクイザル(RPE細胞のMHCの型と一致する型を持つ個体と不一致の個体)の網膜に移植し、それぞれの個体の拒絶反応の有無を調べた。この結果、MHCの型が不一致のカニクイザルでは網膜に拒絶反応が起きた一方で、MHCの型が一致のカニクイザルでは6カ月経過後も拒絶反応は起こらなかった。
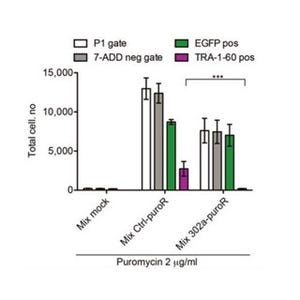
次に、ヒトiPS細胞からRPE細胞(少なくともHLA-A、HLA-B、HLA-DRB1の3座がホモ接合体)を分化・誘導し、そのRPE細胞と、ヒト血液から分離した末梢血単核球(PBMC)およびCD4陽性T細胞をそれぞれ共培養し、試験管内で免疫応答を調べた。この結果、HLAの型が不一致のPBMCとRPE細胞の組み合わせによる共培養では、コントロールに比べて、T細胞、B細胞などの炎症細胞が増加した一方、HLAの型が一致の組み合わせによる共培養では増加しなかった。これにより、炎症細胞はHLA不一致のRPE細胞を認識し、HLA一致のRPE細胞を認識しないことがわかった。
同研究グループは今回の結果について、再生医療用iPS細胞ストック由来のドナーとレシピエントのHLAを一致させることで、RPE細胞移植術後の拒絶反応が抑えられる可能性が示されたとしている。