筑波大学と科学技術振興機構(JST)は1月16日、米ミシガン大学との共同研究により、抗生物質の服用によって増殖した腸内の真菌(カビ)がぜん息を悪化させるメカニズムを解明し、マウスを使った実験によりぜん息を軽快させることにも成功したと共同で発表した。
成果は、筑波大の渋谷彰 教授、ミシガン大のヌネツ教授らの国際共同研究チームによるもの。研究はJST課題達成型基礎研究の一環として行われたもので、詳細な内容は米国東部時間1月15日付けで米国科学誌「Cell Host and Microbe」のオンライン速報版に掲載された。
ヒトの腸管内には、500種類以上、総計100兆個以上の腸内細菌が共生している。腸内細菌は、腸管からの栄養吸収、腸の免疫、病原体の感染の予防などに働いており、近年、ヒトは単体で存在しているのではなく、そうした細菌と共生することで存在していられることがわかってきた。
そのため、遺伝的要因、食餌などを含むライフスタイル、病原体の侵入などや種々の医療的処置などによって腸内細菌のバランスが乱れると、クローン病や潰瘍性大腸炎を初めとする炎症性腸疾患などの原因となってしまう可能性がある。さらに近年になって、腸内細菌のバランスの乱れは、腸管への影響どころでは済まず、全身にも影響を及ぼし、肥満、糖尿病、アトピー、ぜん息などの疾患さえも生じることが知られるようになり、大きな注目を浴びるようになってきた。しかし、どのようなメカニズムでこれらの腸管外の疾患が起きるかについては、ほとんど明らかにされていなかったのである。
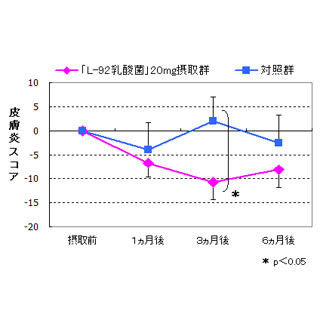
今回の研究では、腸内細菌のバランスの乱れが、なぜぜん息などのアレルギーを引き起こすのかという疑問を明らかにするため、研究チームはまずマウスに5種類の抗生物質をそれぞれ2週間にわたって経口で投与した。その上で、アレルゲンである「パパイン」やダニ抗原の吸入によりぜん息を発症させ、その病態が観察されたのである。その結果、ある種の抗生物質を投与したマウスでは、それ以外の抗生物質を投与したマウスや抗生物質を投与しないマウスに比べ、気道内の炎症が有意に強く、ぜん息症状がより重篤になることが見出された(画像1・2)。
抗生物質というと、微生物が原因で起きる疾病には何でも効くようなイメージがあるが、実は特定の細菌に対してのみ有効な薬であり、ウイルスや真菌に対しては効果がない。また複数種の細菌に感染している場合は、複数の抗生物質を服用する必要があり、万能ではないのだ。
そこで、ぜん息症状が強く出たマウスとそれ以外のマウスで、腸内細菌の変化の違いが比較された。その結果、ぜん息症状が強く出たマウスでは、腸管内で真菌の1種であるカンジダが異常に増殖している一方、乳酸菌などの一部の細菌が減少していることが見出されたのである。これらの結果から、抗生物質の投与によっていわゆる善玉菌が減少し、その結果増殖した悪玉菌であるカンジダが、ぜん息が重篤化する原因となっていることが推察されたというわけだ(画像3・4)。
真菌というと、細菌の仲間のような気がするが、カビのことである。ヒトの疾患に関わるものとしては、前述のカンジダのほか、白癬菌(水虫、たむしなど)、クリプトコッカス、アスペルギルスなどが代表的だ。空気中に胞子が浮遊して感染する場合が多く、通常は肺や皮膚から感染が始まるが、薬や病気による免疫機能の低下がない限り、真菌感染症が重症化することは希である。
ただし、カンジダなど、一部の真菌は体表面や腸内に常在しているものもあるが、その増殖を抑制している善玉細菌が、抗生物質の服用により死滅すると、真菌の増殖に歯止めがかからなくなってしまう薬がマイナスに働いてしまうケースもあるというわけだ。
次に、腸管内カンジダがどのようなメカニズムでぜん息を重篤化させたのかについての解析が行われた。これまで、カンジダなどの真菌は、生理活性物質「プロスタグランジンE2(PGE2)」を産生することが知られていた。プロスタグランジンは人間のさまざまな組織や器官で認められる強力な生理活性物質で、10種類以上に分類される。アスピリンなどの抗炎症剤の多くは、プロスタグランジンの生成を抑制することによって効果を示す仕組みだ。その1つであるPGE2は、平滑筋収縮、末梢血管拡張、発熱・痛覚伝達、骨新生・骨吸収などの作用が知られている。
実際に、抗生物質を投与し腸管内にカンジダが増殖しているマウスの血液中や肺の気道内ではPGE2が、抗生物質を投与していないマウスに比較し、およそ2倍まで増加していることが確認された。しかし、マウスに抗真菌剤を投与してカンジダを減少させると、血液中や気道内のPGE2の値は抗生物質を投与していないマウスと同様の値に戻ったのである(画像5・6)。
また、PGE2を産生できない遺伝子改変マウスにおいても抗生物質の投与により、血液中や肺の気道内のPGE2が増加することが確認された。以上の結果から、カンジダからPGE2が産生され、血液を介して肺まで達していることが判明したというわけだ。
さらに、抗生物質によりカンジダが増殖しているマウスの気道内では、炎症を引き起こすタイプの「M2型マクロファージ」が増加していることが見出された。また、抗生物質を投与していないマウスにPGE2を投与すると、気道内でM2型マクロファージが増加し、ぜん息が重篤化することも確認されたのである(画像7~9)。以上の結果から、PGE2が肺内でM2型マクロファージを増加させていることが判明した。
貪食細胞のマクロファージには、M1とM2の2種類があり、M2型マクロファージは、ヘルパーT細胞の1種の「Th2細胞」に応答して寄生虫感染、アレルギー応答、脂肪代謝、創傷治癒、がん転移などに関与していると考えられている。またM1型マクロファージは、Th1細胞に応答して細菌、ウイルスの感染時に活性化し、それらの病原体の排除に重要な「サイトカイン」(細胞間でやり取りされる多様な生理活性を持つタンパク質の1種)を産生すると考えられている。
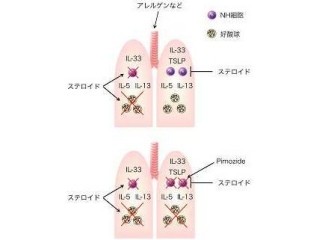
以上の結果をまとめると、以下のようになる(画像10)。(1)ある種の抗生物質の服用により、腸管内でカンジダが増殖する。(2)カンジダからPGE2が産生され、血液を介して肺に到達する。(3)肺内でPGE2がM2型マクロファージを増加させる。(4)増加したM2型マクロファージがぜん息などのアレルギー性炎症を悪化させる。
また、ぜん息の治療としてカンジダの増殖を阻止する抗真菌剤「5FC」、PGE2の産生阻害剤「Asp」、あるいはM2型マクロファージの活性化阻害剤「SAP」などを、抗生物質が投与済みのマウスにそれぞれ投与されたところ、いずれにおいてもぜん息が軽快することが示された(画像11~13)。
アレルギー疾患を代表する花粉症、ぜん息、アトピー性皮膚炎の罹患率は、それぞれ20%、10%、5~10%と、近年増加の一途を辿っている。世界的にもおよそ25%の人がアレルギー疾患に罹患しているとされ、その克服は人類の健康・福祉にとってはもちろんのこと、社会的にも喫緊の課題だ。
アレルギー疾患の発症は、遺伝的素因や環境要因など、さまざまな複合的な因子により発症することが知られているが、その中には腸内細菌のバランスの乱れによる真菌の増殖に起因するものが含まれている可能性が考えられるという。これらの患者では、上記の抗真菌剤、PGE2産生阻害剤、あるいはM2型マクロファージ活性化阻害剤などが効果を示すと考えられるとした。
また真菌の増殖がなくとも、種々の炎症などによってPGE2が炎症組織から産生されることが知られているので、アレルギーによる炎症自体でもPGE2が増加し、これがM2マクロファージを活性化し、悪循環によってさらにアレルギーを増悪させている可能性も疑われるという。
このような患者ではPGE2産生阻害剤が有効である可能性もあるが、一方でPGE2阻害剤自体がぜん息を引き起こすことも知られているので、さらなる研究が必要だとした。また、M2型マクロファージ活性化阻害剤なども効果を示すと考えられるという。これらは、これまでまったく知られていなかった新しい発想のアレルギー疾患の有用な治療法となりうるものと考えられるとする。なお今回の研究成果は、抗生物質の投与による腸内細菌のバランスの乱れがアレルギー性疾患を悪化させたメカニズムを解明したものだ。