名古屋大学(名大)は10月11日、神経線維の主要な細胞骨格である微小管の成長には、精神・神経疾患に関与するタンパク質である細胞骨格「セプチン」と微小管就職酵素「HDAC6」の相互作用が必要であることを見出したと発表した。
同成果は、同大大学院理学研究科の木下専 教授ならびに上田(石原)奈津実 助教、同医学系研究科の宮田卓樹 教授、東京大学大学院医学系研究科の尾藤晴彦 教授らによるもの。詳細は、英国科学誌「Nature Comunications」に英国時間10月11日に掲載される予定。
ヒトの脳は神経細胞(ニューロン)が神経線維を通じて連絡を取り合うことで構成されているが、その神経線維は胎児期と生後発達期に爆発的に伸長・分岐し、その総延長距離は100万kmに及ぶと言われている。個々のニューロンが神経線維を伸ばすためには、繊維の芯となる「細胞骨格」、すなわち微小管の先端にタンパク質「チューブリン」を付加させて、微小管を成長させることが必要となる・
このチューブリンがアセチル化などの化学的修飾を受けると、微小管が安定する反面、安定化しすぎると分解によりリサイクルされるチューブリンの供給が減り、微小管の成長が鈍化することとなることから、微小管の安定化を適度に解除する「脱アセチル化」も重要となるが、このバランスをコントロールする仕組みは良くわかっていなかった。
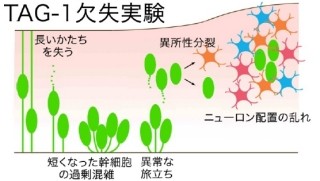
今回、研究グループは研究から、神経細胞の主要な脱アセチル化酵素「BDAC6」がアセチル化チューブリンに効率よく結合して脱アセチル化するには もう1つの細胞骨格「セプチン」が必要であることを突き止めた。具体的には、マウスを用いた実験にて、ニューロンの中に散在する短いフィラメントであるセプチンを欠乏させたところ、HDAC6を阻害したときと同様に微小管が過剰にアセチル化(安定化)して成長が鈍り、神経線維が伸びなくなることを、マウスの脳内ならびに試験管内の両方で確認したという。
なお、今回の成果について研究グループでは、セプチンとHDAC6の相互作用とその生理的意義が示されたことにより、両者が関与する精神・神経疾患への理解が深まることが期待されるとコメントしている。